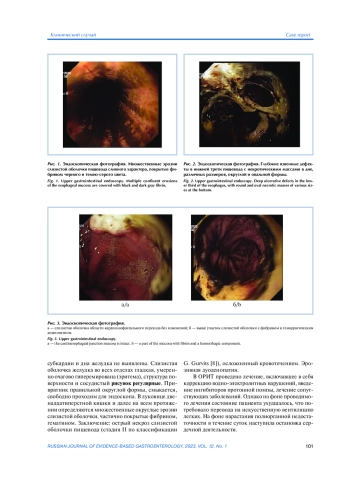
Острый некроз слизистой оболочки пищевода или «черный пищевод» — редкое, остро возникающее заболевание, характеризующееся изолированным поражением слизистой оболочки пищевода, клиническими признаками кровотечения в сочетании с тяжелыми метаболическими нарушениями. Диагноз можно установить по данным эндоскопического обследования верхних отделов желудочно-кишечного тракта. В данной статье представлены случаи эндоскопической диагностики данного заболевания у 5 пациентов, которые госпитализированы в клинику с диагнозом желудочно-кишечного кровотечения. При эндоскопическом исследовании выявлен острый некроз слизистой оболочки пищевода, отмечено отсутствие изменений в зоне пищеводно-желудочного перехода. Эрозивно-язвенные изменения желудка и двенадцатиперстной кишки диагностированы у всех пациентов. У 4 пациентов имелась тяжелая сопутствующая патология (артериальная гипертензия, сахарный диабет, ишемическая болезнь сердца). В 80% случаев имело место злоупотребление алкоголем. Во всех случаях пациентам проводилось лечение как основного синдрома (с применением высоких доз ингибиторов протонной помпы), так и сопутствующей патологии. Хороший эффект получен в трех случаях. Двое пациентов скончались на фоне прогрессирования полиорганной недостаточности. Вероятность острого некроза слизистой оболочки пищевода следует учитывать в процессе дифференциальной диагностике при наличии симптомов одинофагии и желудочно-кишечного кровотечения у пациентов, поступающих в стационар.
Идентификаторы и классификаторы
Острый некроз слизистой оболочки пищевода (ОНСОП) или «черный пищевод» — заболевание, характеризующееся изолированным поражением нижней трети пищевода, с характерной эндоскопической картиной, возникающей в верхних отделах желудочно-кишечного тракта не связанной с приемом агрессивных и едких веществ [1—3]. Типичные изменения при этом состоянии чаще имеют диффузный характер, циркулярное поражение или вид продольно ориентированных полос слизистой оболочки, которая приобретает серо-черную окраску, с четкой границей патологического процесса по линии эзофагогастрального перехода [4]. Впервые это состояние описано R. W. Postlethwait и A. W. Musser в 1974 г. [5].
Если у вас возникли вопросы или появились предложения по содержанию статьи, пожалуйста, направляйте их в рамках данной темы.
Список литературы
1. Gurvits GE, Cherian K, Shami MN, Korabathina R, El-Nader EM, Rayapudi K, Gandolfo FJ, Alshumrany M, Patel H, Chowdhury DN, Tsiakos A. Black Esophagus: New Insights and Multicenter International Experience in 2014. Digestive Diseases and Sciences. 2015;60(2):444-453. DOI: 10.1007/s10620-014-3382-1
2. Rodrigues BD, Dos Santos R, da Luz MM, Chaves E Silva F, Reis IG. Acute esophageal necrosis. Clinical Journal of Gastroenterology. 2016;9(6):341-344. DOI: 10.1007/s12328-016-0692-1
3. Rehman O, Jaferi U, Padda I, Khehra N, Atwal H, Parmar M. Epidemiology, Pathogenesis, and Clinical Manifestations of Acute Esophageal Necrosis in Adults. Cureus. 2021;13(7):e16618. DOI: 10.7759/cureus.16618
4. Lamers CR, Mares WGN, Bac DJ. Black esophagus: a case series and literature review of acute esophageal necrosis. Scandinavian Journal of Gastroenterology. 2018;53(10-11):1421-1424. DOI: 10.1080/00365521.2018.1513064
5. Postlethwait RW, Musser AW. Changes in the esophagus in 1,000 autopsy specimens. The Journal of Thoracic and Cardiovascular Surgery. 1974;68(6):953-956.
6. Sheikh AB, Mirza S, Abbas R, Javed N, Nguyen A, Hanif H, Farooq A. Acute Esophageal Necrosis: An In-depth Review of Pathogenesis, Diagnosis and Management. Journal of Community Hospital Internal Medicine Perspectives. 2022;12(1):96-103. DOI: 10.55729/2000-9666.1020
7. Schizas D, Theochari NA, Mylonas KS, Kanavidis P, Spartalis E, Triantafyllou S, Economopoulos KP, Theodorou D, Liakakos T. Acute esophageal necrosis: A systematic review and pooled analysis. World Journal of Gastrointestinal Surgery. 2020;12(3):104-115. DOI: 10.4240/wjgs.v12.i3.104
8. Gurvits GE, Shapsis A, Lau N, Gualtieri N, Robilotti JG. Acute esophageal necrosis: a rare syndrome. Journal of Gastroenterology. 2007;42(1):29-38. DOI: 10.1007/s00535-006-1974-z
9. Averbukh LD, Mavilia MG, Gurvits GE. Acute Esophageal Necrosis: A Case Series. Cureus. 2018;10(3):e2391. DOI: 10.7759/cureus.2391
10. Kroner PT, Chirila R, Purcarea MR, Tribus L, Wadei HM. Acute esophageal necrosis following kidney transplantation. Journal of Medicine and Life. 2021;14(2):284-286. DOI: 10.25122/jml-2021-0024
11. Yasuda H, Yamada M, Endo Y, Inoue K, Yoshiba M. Acute necrotizing esophagitis: role of nonsteroidal anti-inflammatory drugs. Journal of Gastroenterology. 2006;41(3):193-197. DOI: 10.1007/s00535-005-1741-6
12. Julián Gómez L, Barrio J, Atienza R, Fernández-Orcajo P, Mata L, Saracibar E, de la Serna C, Gil-Simón P, Vallecillo MA, Caro Patón A. Acute esophageal necrosis: An underdiagnosed disease. Revista Espanõla de Enfermedades Digestivas. 2008;100(11):701-705. DOI: 10.4321/s1130-01082008001100006
13. Kim SM, Song KH, Kang SH, Moon HS, Sung JK, Kim SH, Kim KB, Lee SW, Cho YS, Bang KB. Evaluation of prognostic factor and nature of acute esophageal necrosis. Medicine (Baltimore). 2019;98(41):e17511. DOI: 10.1097/MD.0000000000017511
14. Goldenberg SP, Wain SL, Marignani P. Acute necrotizing esophagitis. Gastroenterology. 1990;98:493-496. DOI: 10.1016/0016-5085(90)90844-q
15. Dias E, Santos-Antunes J, Macedo G. Diagnosis and management of acute esophageal necrosis. Annals of Gastroenterology. 2019; 32(6):529-540. DOI: 10.20524/aog.2019.0418
16. Tomoda Y, Yoshimura D, Hayashida E, Tanaka K. Black Oesophagus-acute esophageal necrosis. QJM. 2021;114(1):56-57. DOI: 10.1093/qjmed/hcaa143
17. Day A, Sayegh M. Acute oesophageal necrosis: a case report and review of the literature. International Journal of Surgery. 2010; 8(1):6-14. DOI: 10.1016/j.ijsu.2009.09.014
18. Endo T, Sakamoto J, Sato K, Takimoto M, Shimaya K, Mikami T, Munakata A, Shimoyama T, Fukuda S. Acute esophageal necrosis caused by alcohol abuse. World Journal of Gastroenterology. 2005;11(35):5568-5570. DOI: 10.1016/j.ijsu.2009.09.014
19. Siddiqi A, Chaudhary FS, Naqvi HA, Saleh N, Farooqi R, Yousaf MN. Black esophagus: a syndrome of acute esophageal necrosis associated with active alcohol drinking. BMJ Open Gastroenterology. 2020;7(1):e000466. DOI: 10.1136/bmjgast-2020-000466
20. Augusto F, Fernandes V, Cremers MI, Oliveira AP, Lobato C, Alves AL, Pinho C, de Freitas J. Acute necrotizing esophagitis: a large retrospective case series. Endoscopy. 2004;36(5):411-415. DOI: 10.1055/s-2004-814318
21. Vien LP, Yeung HM. Acute Esophageal Necrosis (Gurvits Syndrome): A Rare Complication of Diabetic Ketoacidosis in a Critically Ill Patient. Case Reports in Medicine. 2020;2020:5795847. DOI: 10.1155/2020/5795847
22. Deliwala SS, Bala A, Haykal T, Elbedawi MM, Bachuwa G, Gurvits GE. Acute Esophageal Necrosis (Gurvits Syndrome) Presenting as Globus and Altered Phonation. The American Journal of Case Reports. 2020;21:e926019. DOI: 10.12659/AJCR.926019 geal necrosis masquerading acute coronary syndrome. Autopsy and Case Reports. 2020;10(1):e2019136. DOI: 10.4322/acr.2019.136
24. Tsokos M, Herbst H. Black oesophagus: a rare disorder with potentially fatal outcome. A forensic pathological approach based on five autopsy cases. International Journal of Legal Medicine. 2005; 119(3):146-152. DOI: 10.1007/s00414-004-0509-5
25. Sandhu S, Wang T, Prajapati D. Acute esophageal necrosis complicated by refractory stricture formation. JGH Open. 2021;5(4):528-530.
Выпуск
Другие статьи выпуска
Цель исследования. Представить клиническое наблюдение больших участков гетеротопии слизистой оболочки желудка у ребенка в верхней и нижней третях пищевода.
Клиническое наблюдение. Мальчик 13 лет с диагнозом трисомия по 21 паре хромосом (синдром Дауна, аутоиммунный тиреоидит (гипертрофическая форма), задержка психоречевого развития, нарушение сердечного ритма) впервые обратился в ФГАУ «НМИЦ здоровья детей» Минздрава России с жалобами на периодическую боль в животе и отрыжку. По данным рентгеноконтрастного исследования установлено отсутствие гастроэзофагеального рефлюкса. Выполнена эзофагогастродуоденоскопия (ЭГДС): в верхней и нижней трети пищевода выявлено много участков гетеротопированной слизистой оболочки, максимальный размер которых достигал 3×2 см. Выполнена биопсия нескольких участков гетеротопии. При морфологическом исследовании выявлено, что гетеротопированная ткань соответствует слизистой оболочке желудка. Через 8 месяцев при выполнении контрольной ЭГДС обнаружено, что участки гетеротопии без изменений. В настоящее время пациент получает антирефлюксную и антисекреторную терапию.
Заключение. Гетеротопия слизистой оболочки желудка в пищеводе — частый порок развития. Чаще всего участки эктопии имеют небольшой размер и не дают клинической картины. Однако встречаются «большие участки» гетеротопии, которые могут иметь клинические проявления, такие как боль, изжога и дисфагия. Крупные участки гетеротопии (в нижней трети пищевода) необходимо дифференцировать с пищеводом Баррета. В данном случае не возникло сомнений, что у данного пациента гетеротопия, а не метаплазия слизистой оболочки. Это подтверждено макроскопической картиной («оторванность» от Z-линии, нециркулярное расположение), а также отсутствием гастроэзофагеального рефлюкса по данным рентгеноконтрастного исследования. Следует обратить внимание на то, что у пациентов с гетеротопией слизистой оболочки желудка существует риск малигнизации. Учитывая онконастороженность, необходимо выполнять контрольную эзофагогастродуоденоскопию и оценивать участки гетеротопии в динамике.
Цель исследования. Обобщить имеющиеся данные о патогенезе внекишечных проявлений (ВКП) воспалительных заболеваний кишечника (ВЗК) с целью более полного понимания и формирования патогенетической концепции воспалительных заболеваний кишечника и ведения пациентов с данной патологией.
Материал и методы. Проведен поиск статей в базе данных PubMed за период с 1965 по 2021 г. с описанием случаев возникновения ВКП ВЗК, существующих и перспективных методов их лечения. Выполнен литературный обзор.
Результаты. Патогенез развития ВКП является мультифакториальным, он ассоциирован с обеднением кишечной микрофлоры, опосредован выработкой системных аутоантител и связан с повышенным риском развития онкологических заболеваний.
Заключение. Ввиду обширности проявлений воспалительных заболеваний кишечника необходим мультидисциплинарный и индивидуальный подход к ведению пациентов, а также есть основания для дальнейшего изучения концепций развития данной группы заболеваний и их системных проявлений, что, в свою очередь, влияет на подбор и поиск таргетной биологической терапии.
С начала XXI века на фоне промышленной революции в индустрии продуктов питания и напитков наблюдается тенденция к увеличению количества скрытых подсластителей, в основном в виде сахарозы и кукурузного сиропа с высоким содержанием фруктозы. В отличие от глюкозы, метаболизм фруктозы, поступившей с пищей, происходит главным образом в печени, что позволяет считать этот орган и протекающие в нем процессы ключом к пониманию неблагоприятного влияния фруктозы на организм. На сегодняшний день накоплены данные, подтверждающие, что именно фруктоза является фактором, способствующим развитию метаболического синдрома. В настоящем обзоре рассмотрены потенциальные механизмы взаимосвязи избыточного потребления фруктозы и развития ожирения и неалкогольной жировой болезни печени.
Цель обзора. Провести краткий анализ и обсудить основные положения обновленной версии Чикагской классификации нарушений моторной функции пищевода (версия 4.0), опубликованной впервые в 2021 г. в журнале Neurogastroenterology and Motility (Нейрогастроэнтерология и моторика).
Основные положения. Чикагская классификация версия 4.0 представляет собой обновленную классификационную схему нарушений моторики пищевода с использованием показателей манометрии высокого разрешения. Над разработкой новой классификации в течение двух лет работали 7 экспертных групп (52 эксперта в области манометрии пищевода из разных стран). Ключевые обновления Чикагской классификации версии 4.0 включают описание более тщательной и расширенной методики проведения исследования, использование провокационных тестов. В отличие от предыдущей версии, Чикагская классификация версия 4.0 подразумевает обязательное описание исходных манометрических параметров пищеводно-желудочного соединения. Кроме того, внесены обновления и более строгие критерии в диагностику нарушений проходимости пищеводно-желудочного соединения, неэффективной моторики пищевода. В зависимости от наличия и выраженности клинических симптомов, результатов провокационных тестов в новой версии Чикагской классификации допускается выдача заключения после проведения манометрии пищевода как в виде окончательного, так и виде неподтвержденного манометрического диагноза.
Заключение. Основные положения Чикагской классификации нарушений моторики пищевода 4-го пересмотра в целом подтвердили предыдущую версию данного документа. Изменения, внесенные советом экспертов в обновленную версию Чикагской классификации, касались расширенного применения провокационных тестов для обеспечения более точной диагностики заболеваний, сопровождающихся обструкцией нижнего пищеводного сфинктера. Введены новые диагностические критерии для стандартизированной диагностики нарушений моторики пищевода.
Информированное добровольное согласие (ИДС) на проведение эндоскопического вмешательства — это медико-юридический документ, целью которого является урегулирование взаимоотношений между пациентом, врачом и клиникой. Этот документ является информационным, раскрывающим суть вмешательства для пациента, в том числе риски, ассоциированные с вмешательством. Наличие и детализация рисков, связанных с оказанием медицинской помощи, должны быть обязательной составляющей ИДС, о чем говорит Федеральный закон от 21.11.11 №323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации». Отсутствие стандартизованного ИДС по специальности «эндоскопия», отвечающего современным юридическим стандартам, послужило причиной организации серии мероприятий с целью его формирования под эгидой Ассоциации врачей-экспертов качества медицинской помощи. Результатом этого мероприятия явилось создание ИДС по основным направлениям эндоскопии, в том числе по верхним отделам желудочно-кишечного тракта, в котором одной из составляющих является стандартизованная информация о структуре возможных осложнений, связанных как с диагностическим, так и с лечебным вмешательством.
Цель исследования. Изучение причин высокого удельного веса случаев посмертной диагностики гепатоцеллюлярного рака (ГЦР), влияния демографических показателей на вероятность посмертного установления диагноза.
Материал и методы. В ретроспективное наблюдательное исследование включили данные больных ГЦР, жителей Свердловской области, диагноз у которых был установлен в 2015—2021 гг. Оценивали удельный вес случаев посмертной диагностики. Сравнивали показатели больных с прижизненным (325 пациентов) и посмертным диагнозом (351 пациентов). Последние были разделены на две группы: 227 пациентов, которые обращались в течение года до смерти за медицинской помощью, и 124 пациента, которые не обращались.
Результаты. Удельный вес посмертной диагностики ГЦР в течение последних 7 лет составил 46,3%. Вероятность посмертной диагностики была выше в 1,57 раза у больных старше 65 лет (p<0,001), в 1,19 раза — у лиц женского пола (p=0,02), в 2,1 раза — при отсутствии цирроза печени (p<0,001). Место жительства достоверно не влияло на вероятность прижизненной диагностики. Более 60% пациентов с посмертной диагностикой обращались за медицинской помощью в течение года до смерти, и онкологический диагноз у них не был заподозрен. Большинство таких больных получили плановую амбулаторную помощь терапевтического профиля.
Заключение. Большая доля посмертного выявления ГЦР диктует необходимость реализации программ скрининга среди групп риска и повышения онкологической настороженности у врачей общей лечебной сети.
Более чем у 75% пациентов с болезнью Крона в течение жизни возникает потребность как минимум в одном хирургическом вмешательстве по поводу осложнений данного заболевания. В послеоперационном периоде для своевременной активизации и восстановления пациента необходимо адекватное обезболивание. Однако у данных пациентов интенсивность послеоперационного болевого синдрома гораздо выше, чем у пациентов онкологического или общего хирургического профиля, что связано с нерегулируемым воспалением, характерным для болезни Крона.
Цель исследования. Сравнить болевой синдром после илеоцекальной резекции при болезни Крона и правосторонней гемиколэктомии по поводу рака слепой кишки.
Материал и методы. В исследование ретроспективно включены 2 группы пациентов по 22 человека (основная — оперированные по поводу осложнений болезни Крона в объеме лапароскопической илеоцекальной резекции, контрольная — оперированные по поводу рака слепой кишки в объеме лапароскопической правосторонней гемиколэктомии) в период с 2015 по 2021 г. У всех пациентов в раннем послеоперационном периоде выполнена оценка интенсивности болевого синдрома по визуальной аналоговой шкале и уровня C-реактивного белка в крови.
Результаты. Интенсивность болевого синдрома различалась у пациентов основной и контрольной групп статистически значимо в первые 3 суток после операции (p=0,03), статистически незначимо — в последующем (p=0,13). Уровень C-реактивного белка у пациентов основной группы в раннем послеоперационном периоде был выше, чем у пациентов контрольной группы (p<0,05). Опиоидные аналгетики у пациентов с болезнью Крона использовались статистически значимо чаще (p=0,03).
Выводы. У пациентов с болезнью Крона значительно выше болевой синдром и уровень C-реактивного белка в раннем послеоперационном периоде по сравнению с пациентами контрольной группы, также выявлена корреляция между интенсивностью боли и уровнем воспалительных маркеров.
Цель исследования. Изучить уровни интерлейкина-10 (IL-10) у пациентов с гепатитом и циррозом печени алкогольной этиологии.
Материал и методы. Исследование выполнено по протоколу контролируемого исследования методов диагностики случай—контроль. Обследовано 18 пациентов с хроническим гепатитом, 41 пациент с циррозом печени алкогольной этиологии и 15 практически здоровых лиц.
Результаты. Установлено, что уровень IL-10 у пациентов с циррозом печени (3,15; 0,37—9,2 пг/мл) выше, чем у контрольной группы (0; 0—2,7 пг/мл, p<0,01). Уровень IL-10 у пациентов с циррозом печени и пациентов с хроническим гепатитом (0; 0—5,92 пг/мл, p>0,05), как и у пациентов с хроническим гепатитом и контрольной группе статистически не различаются (p>0,05). У пациентов с циррозом печени класса B и C по Child-Puge уровень IL-10 статистически значимо выше (3,15; 1,76—8,24 пг/мл и 6,16; 0,37—12,4 пкг/мл соответственно), чем у пациентов с циррозом печени класса A по Child-Puge (0,37; 0—0,83 пг/мл, p<0,05). У пациентов с прогрессирующими формами цирроза печени (класс B и C) уровень IL-10 статистически значимо выше, чем у пациентов с хроническим гепатитом и циррозом печени класса A (p<0,05). У пациентов с циррозом печени установлены корреляции средней силы IL-10 с уровнем Fib4 (r=0,54), APRI (r=0,58), Forns (r=0,64), эритроцитов (r= –0,6), гемоглобина (r= –0,6), тромбоцитов (r= –0,63), лимфоцитов (r= –0,52), сегментоядерных нейтрофилов (r=0,47), протромбинового индекса (r= –0,59), активированного частичного тромбопластинового времени (r=0,37).
Заключение. Интерлейкин-10, предупреждая процессы воспаления и некроза, а также стимулируя регенеративные процессы, является важным противовоспалительным цитокином, участвующим в патогенезе алкоголь-зависимых заболеваний печени.
Цель исследования. Оценить способы лечения повреждений и стриктур общего желчного протока на основе сохранения оптимального кровоснабжения зоны анастомоза.
Материал и методы. Изучено строение стенок желчного пузыря, общего печеночного и желчного протоков. Проведен анализ лечения 117 пациентов с травмами и стриктурами общего желчного протока. Мужчин было 28 (23,9%), женщин — 89 (76,1%), возраст — от 20 до 79 лет. «Свежая» травма протоков была у 58 (49,6%) пациентов, стриктуры — у 59 (50,4%). При обнаружении «свежей» травмы общего желчного протока выполняли восстановительную операцию — гепатикоэнтеростомию на сменном транспеченочном дренаже по Гетцу. При стриктурах формирование каркасного анастомоза проводили при диаметре общего желчного протока менее 15 мм, а при диаметре более 15 мм — бескаркасного анастомоза.
Результаты. Особенностями морфологического строения желчного пузыря и внепеченочных желчных протоков являются отсутствие подслизистой оболочки и хорошо развитая субсерозная оболочка, в которой расположены сосуды, кровоснабжающие стенки органов. У 84,4% пациентов с травмами и стриктурами общего желчного протока с учетом сохранения оптимального кровоснабжения зоны анастомоза формирование гепатикоэнтероанастоза выполнено на сквозном транспеченочном дренаже по Гетцу, а у 15,6% пациентов с шириной общего желчного протока более 15 мм — бескаркасное наложение гепатикоэнтеро- и гепатикодуоденоанастоза.
Заключение. При выполнении операций на сквозном транспеченочном дренаже по Гетцу послеоперационная летальность составляет 5,2%, а при стриктурах — 3,4%. В отдаленные сроки после гепатикоэнтеростомии на сменном дренаже по Гетцу анастомотические стриктуры развиваются у 1,37% пациентов, а после бескаркасной гепатикоэнтеростомии и гепатикодуоденостомии — у 6,67%.
Распространенность язвенной болезни среди взрослого населения достигает 10%, причем язвенная болезнь желудка (ЯБЖ) характерна для лиц в возрасте 55—70 лет. ЯБЖ является мультифакториальной патологией, в развитие которой большой вклад вносят наследственные факторы и инфекция H. pylori.
Цель исследования. Изучить роль полиморфных вариантов генов-кандидатов (rs2294008 гена PSCA, rs6136 гена SELP, rs505922, rs8176720, rs2519093, rs507666 гена АВО, rs651007, rs579459, rs649129 гена ABO/RF00019) в развитии H. pyloriпозитивной ЯБЖ.
Материал и методы. В настоящем исследовании участвовали 98 больных H. pylori-позитивной ЯБЖ и 347 индивидуумов контрольной группы, оценка регуляторного потенциала отобранных для изучения SNPs проводилась с помощью интернет-ресурсов HaploReg v4.1, PolyPhen-2, GTEx Portal, генотипирование осуществлено молекулярно-генетическим методом с применением полимеразной цепной реакции. Анализ ассоциаций проведен методом логистической регрессии в рамках аллельной, аддитивной, доминантной и рецессивной генетических моделей.
Результаты. Аллель C гена SELP (rs6136) является генетическим фактором риска развития H. pylori-позитивной ЯБЖ (ОШ=1,66; 95% ДИ 1,02—2,71; p=0,041; pperm=0,042). Полиморфизм rs6136 имеет выраженный регуляторный потенциал, является несинонимичным, рисковый в отношении развития H. pylori-позитивной ЯБЖ аллель C rs6136 ассоциирован с повышенной экспрессией гена F5 и снижением альтернативного сплайсинга гена BLZF1.
Выводы. Генетическим фактором риска развития H. pylori-позитивной язвенной болезни желудка является аллель C гена SELP (rs6136).
Цель исследования. Оценка результатов применения металлических саморасправляющихся стентов у пациентов с дисфагией злокачественного генеза.
Материал и методы. За период 2006—2021 гг. установка металлических саморасправляющихся стентов при злокачественной дисфагии проведена 216 пациентам (средний возраст 62,03±11,61 года; 163 мужчины и 53 женщины). У 111 пациентов был рак пищевода, у 53 — рак кардиального отдела желудка с переходом на пищевод, у 23 — компрессия из-за сдавления извне при других опухолях, у 28 — рецидив рака после операций на пищеводе и желудке, у 1 — нейрофиброматоз легких и средостения.
Результаты. Осложнений при установке стента не было. Осложнения в послеоперационном периоде разделены на ранние (до двух недель после установки) — 12 пациентов (исключая болевой синдром), и поздние (свыше двух недель после установки) — 45 пациентов. Два пациента погибли из-за массивного кровотечения. Большинство осложнений успешно устранены с использованием эндоскопических методов, в том числе путем стентирования по типу «стент в стент», стентирования трахеи из-за прорастания опухоли.
Выводы. Установка стентов у пациентов с дисфагией злокачественного генеза является методом выбора. Стентирование под рентгенологическим контролем может быть применено на этапах освоения метода и при «высокой» локализации проксимального края стеноза. В остальных случаях достаточно эндоскопического контроля. Необходима организация обратной связи врач-пациент или врач-родственник для своевременного выявления и коррекции осложнений. Более 95% осложнений после стентирования могут быть устранены с использованием эндоскопических методов.
Статистика статьи
Статистика просмотров за 2026 год.
Издательство
- Издательство
- МЕДИА СФЕРА
- Регион
- Россия, Москва
- Почтовый адрес
- Издательство «Медиа Сфера», а/я 54, Москва, Россия, 127238
- Юр. адрес
- 127238, город Москва, Дмитровское ш, д. 46 к. 2 стр. 2
- ФИО
- Немцова Нина Валерьевна (ГЕНЕРАЛЬНЫЙ ДИРЕКТОР)
- E-mail адрес
- info@mediasphera.ru
- Контактный телефон
- +7 (495) 4824329