Цель исследования. Оценить способы лечения повреждений и стриктур общего желчного протока на основе сохранения оптимального кровоснабжения зоны анастомоза.
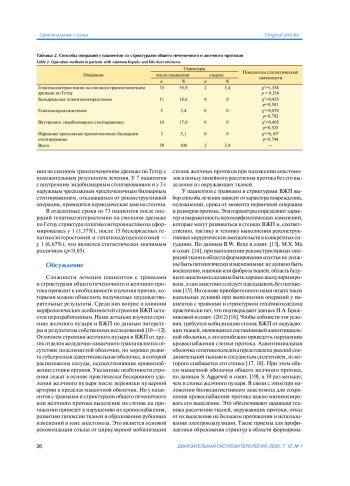
Материал и методы. Изучено строение стенок желчного пузыря, общего печеночного и желчного протоков. Проведен анализ лечения 117 пациентов с травмами и стриктурами общего желчного протока. Мужчин было 28 (23,9%), женщин — 89 (76,1%), возраст — от 20 до 79 лет. «Свежая» травма протоков была у 58 (49,6%) пациентов, стриктуры — у 59 (50,4%). При обнаружении «свежей» травмы общего желчного протока выполняли восстановительную операцию — гепатикоэнтеростомию на сменном транспеченочном дренаже по Гетцу. При стриктурах формирование каркасного анастомоза проводили при диаметре общего желчного протока менее 15 мм, а при диаметре более 15 мм — бескаркасного анастомоза.
Результаты. Особенностями морфологического строения желчного пузыря и внепеченочных желчных протоков являются отсутствие подслизистой оболочки и хорошо развитая субсерозная оболочка, в которой расположены сосуды, кровоснабжающие стенки органов. У 84,4% пациентов с травмами и стриктурами общего желчного протока с учетом сохранения оптимального кровоснабжения зоны анастомоза формирование гепатикоэнтероанастоза выполнено на сквозном транспеченочном дренаже по Гетцу, а у 15,6% пациентов с шириной общего желчного протока более 15 мм — бескаркасное наложение гепатикоэнтеро- и гепатикодуоденоанастоза.
Заключение. При выполнении операций на сквозном транспеченочном дренаже по Гетцу послеоперационная летальность составляет 5,2%, а при стриктурах — 3,4%. В отдаленные сроки после гепатикоэнтеростомии на сменном дренаже по Гетцу анастомотические стриктуры развиваются у 1,37% пациентов, а после бескаркасной гепатикоэнтеростомии и гепатикодуоденостомии — у 6,67%.
Идентификаторы и классификаторы
При травмах внепеченочных желчных протоков (ВЖП) имеется связь локализации повреждения общего печеного и желчного протоков с выполняемым оперативным вмешательством. При желчнокаменной болезни стриктуры терминального отдела общего желчного протока (ductus choledochus) образуются у 13% больных, повреждения при открытой холецистэктомии (ХЭ) — у 1—3%, при лапароскопической ХЭ — у 3,5%, при ХЭ из мини-доступа — у 0,4—1%, при резекции желудка — у 0,1—1,5%. После пересадки донорской печени стриктуры формируются у 5—15% пациентов, после пересадки сегмента печени — у 28— 32%. Дискуссии по вопросу лечения повреждений и стриктур ВЖП способами каркасного и бескаркасного формирования гепатикоэнтероанастомоза продолжаются, что обусловлено сохраняющимися в большой доле случаев осложнениями. Так, несостоятельность швов после формирования гепатикоэнтероанастомоза без каркаса достигает 13% [1], а частота рецидивов стриктур после восстановительной и реконструктивной операции колеблется от 10 до 20% [2, 3]. В нашей стране вклад в развитие билиарной хирургии повреждений желчных протоков и их осложнений внесли В. В. Виноградов и Э. И. Гальперин [4, 5]. В 1951 г. O. Goetze [6] предложил способ сквозного дренирования ВЖП через правую долю печени, сформированный гепатикоэнтероанастомоз, тощую кишку, мобилизованную по Ру, трубкой, концы которой выводятся на поверхность кожи (операция по Гетцу). Преимуществами способа являются декомпрессия внутрипеченочных и ВЖП, снижающая риск несостоятельности гепатикоэнтероанастомоза и желчеистечения, легкая замена, что важно при длительном стоянии дренажа в протоках [7], низкая частота развития стриктуры в сформированном анастомозе при удалении дренажа в сроки не менее, чем через 2 года после установки [8, 9].
Если у вас возникли вопросы или появились предложения по содержанию статьи, пожалуйста, направляйте их в рамках данной темы.
Список литературы
1. Расулов Н.А., Курбонов К.М., Назирбоев К.Р. Оптимизация диагностики и лечения различных типов рубцовых стриктур желчных протоков. Вестник Академии медицинских наук Таджикистана. 2017;2(22):47-50.
Rasulov NA, Kurbonov KM, Nazirboev KR. Optimization of diagnosis and treatment of various types of cicatricial strictures of the bile ducts. Bulletin of the Academy of Medical Sciences of Tajikistan. 2017;2(22):47-50. (In Russ.).
2. Борисов А.Е. Первичные повреждения и рубцовые стриктуры желчных протоков. Руководство по хирургии печени и желчевыводящих путей. Том 2. СПб.: Скифия; 2003;183-268.
Borisov A.E. Pervichnye povrezhdeniya i rubcovye striktury zhelchnyh protokov. Rukovodstvo po hirurgii pecheni i zhelchevyvodyashchih putej. Tom 2. SPb.: Skifiya; 2003;183-268. (In Russ.).
3. Bismuth H, Majno PE. Biliary strictures: classification based on the principles of surgical treatment. World Journal of Surgery. 2001;25(10):1241-1244. DOI: 10.1007/s00268-001-0102-8
4. Виноградов В.В., Вишневский В.А., Кочиашвили В.И. Билиодигестивные анастомозы. М.: Издательство университета дружбы народов имени Патриса Лумумбы; 1972. (In Russ.).
Vinogradov VV, Vishnevsky VA, Kochiashvili VI. Biliodigestivnye anastomozy. M.: Izdatel’stvo universiteta druzhby narodov imeni Patrisa Lumumby; 1972. (In Russ.).
5. Гальперин Э.И., Кузовлев Н.Ф., Карагюлян С.Р. Рубцовые стриктуры желчных протоков. М.: Медицина; 1982.
Galperin EI, Kuzovlev NF, Karagyulyan SR. Rubcovye striktury zhelchnyh protokov. M.: Medicina; 1982. (In Russ.).
6. Goetze O. Transhepatic permanent drainage in high-seated stenosis of the common bile duct. Langenbecks Archiv fur klinische Chirurgie... vereinigt mit Deutsche Zeitschrift fur Chirurgie. 1951;270:97-101.
7. Smith R. Hepaticojejunostomy with transhepatic intubation. The British Journal of Surgery. 1964;51:186-194. DOI: 10.1002/bjs.1800510307
8. Гальперин Э.И., Ветшев П.С. Руководство по хирургии желчных путей. М.: Видар; 2009.
Galperin EI, Vetshev PS. Rukovodstvo po hirurgii zhelchnyh putej. M.: Vidar; 2009. (In Russ.).
9. Praderi R. Choledocostomia Transhepatico. Revista Cirugía del Uruguay. 1961;32.2-3:237-241.
10. Гальперин Э.И., Чевокин А.Ю. “Свежие” повреждения желчных протоков. Хирургия. Журнал им. Н.И. Пирогова. 2010; (10):4-10.
Gal’perin ÉI, Chevokin AIu. Intraoperative injuries of bile ducts. Khirurgiya. Zurnal im. N.I. Pirogova. 2010;(10):4-10. (In Russ.).
11. Hendrickson WF. A study of the musculature of the entire extrahepatic biliary system including than of duodenal portion of the common bile duct and of the sphincter. Bulletin of the Johns Hopkins Hospital. 1898;9:221-232.
12. Кялян Г.П., Азнаурян А.В. Возрастные особенности мышечного слоя желчного протока человека. Морфология. 1995; 108(1):10-12.
Kalyan GP, Aznauryan AV. Age features of the muscular layer of the human bile duct. Morphologiya. 1995;108(1):10-12. (In Russ.).
13. Renz BW, Bösch F, Angele MK. Bile Duct Injury after Cholecystectomy: Surgical Therapy. Visceral Medicine. 2017;33(3):184-190. DOI: 10.1159/000471818
14. Ma MX, Jayasekeran V, Chong AK. Benign biliary strictures: prevalence, impact, and management strategies. Clinical and Experimental Gastroenterology. 2019;18(12):83-92. DOI: 10.2147/CEG.S165016
15. Kukar M, Wilkinson N. Surgical Management of Bile Duct Strictures. The Indian Journal of Surgery. 2015;77(2):125-132. DOI: 10.1007/s12262-013-0972-7
16. Бражникова Н.А., Мерзликин Н.В., Цхай В.Ф., Хлебникова Ю.А., Еськов И.М., Шелепов С.В., Саипов М.Б., Курачева Н.А. Непосредственные результаты корригирующих операций повреждений желчных протоков при холецистэктомиях. Бюллетень сибирской медицины. 2012;11(1):141-149.
Brazhnikova NA, Merzlikin NB, Tskhai VF, Khlebnikova YuA, Yeskov IM, Shelepov SV, Saipov MB, Kuracheva NA. Immediate results of corrective surgeries for bile duct injuries in cholecystectomy. Byulleten’ sibirskoj mediciny. 2012;11(1):141-149. (In Russ.).
17. Борисенко В.Б., Сорокина И.В., Горголь Н.И. Патоморфологическая характеристика холедоха при экспериментальном холестазе. Вестник проблем биологии и медицины. 2014;3(4):261-266.
Borisenko VB, Sorokina IV, Gorgol NI. Pathological characteristics of choledochus in experimental cholestasis. Vestnik problem biologii i mediciny. 2014;3(4):261-266. (In Russ.).
18. Добряков Б.С., Бравве И.Ю., Бородач А.В. Морфофункциональные особенности внепеченочных желчных путей. Сибирское медицинское обозрение. 2010;64(4):21-26.
Dobryakov BS, Bravve IYu, Borodach AV. Morphofunctional features of the extrahepatic biliary tract. Sibirskoe medicinskoe obozrenie. 2010;64(4):21-26. (In Russ.).
19. Aggarwal S, Kumar A, Roy S, Bandhu S. Massive dilatation of the common bile duct resembling a choledochal cyst. Tropical Gastroenterology. 2001;22(4):219-220.
20. Восканян С.Э., Попов М.В., Артемьев А.И., Сушков А.И., Колышев И.Ю., Рудаков В.С., Малышева А.П., Забежинский Д.А. Билиарные анастомотические стриктуры после трансплантации правой доли печени от живого родственного донора: опыт одного трансплантационного центра. Хирургия. Журнал им. Н.И. Пирогова. 2021;(2):5-13.
Voskanyan SE, Popov MV, Artemiev AI, Sushkov AI, Kolyshev IYu, Rudakov VS, Maltseva AP, Zabezhinskiy DA. Bilary anastomotic strictures after right lobe living donor liver transplantation: a single-center experience. Khirurgiya. Zurnal im. N.I. Pirogova. 2021;(2):5-13. (In Russ.). DOI: 10.17116/hirurgia20210215
21. Ikegami T, Shirabe K, Morita K, Soejima Y, Taketomi A, Yoshizumi T, Uchiyama H, Kayashima H, Hashimoto N, Maehara Y. Minimal hilar dissection prevents biliary anastomotic stricture after living donor liver transplantation. Transplantation. 2011; 27;92(10):1147-1151. DOI: 10.1097/TP.0b013e3182336073
22. Kim SH, Kim YK. Living donor right hepatectomy using the hanging maneuver by Glisson’s approach under the upper midline incision. World Journal of Surgery. 2012;36(2):401-406. DOI: 10.1007/s00268-011-1340-z
23. Lin TS, Chen CL, Concejero AM, Yap AQ, Lin YH, Liu CY, Chiang YC, Wang CC, Wang SH, Lin CC, Yong CC, Cheng YF. Section 9. Technical details of microsurgical biliary reconstruction in living donor liver transplantation. Transplantation.2014;97(27) suppl 8:34-36. DOI: 10.1097/01.tp.0000446273.13310.77
24. Shah RJ, Smolkin M, Yen R, Ross A, Kozarek RA, Howell DA, Bakis G, Jonnalagadda SS, Al-Lehibi AA, Hardy A, Morgan DR, Sethi A, Stevens PD, Akerman PA, Thakkar SJ, Brauer BC. A multicenter, U.S. experience of single-balloon, double-balloon, and rotational overtube-assisted enteroscopy ERCP in patients with surgically altered pancreaticobiliary anatomy (with video). Gastrointestinal Endoscopy. 2013;77(4):593-600. DOI: 10.1016/j.gie.2012.10.015
Выпуск
Другие статьи выпуска
Цель исследования. Представить клиническое наблюдение больших участков гетеротопии слизистой оболочки желудка у ребенка в верхней и нижней третях пищевода.
Клиническое наблюдение. Мальчик 13 лет с диагнозом трисомия по 21 паре хромосом (синдром Дауна, аутоиммунный тиреоидит (гипертрофическая форма), задержка психоречевого развития, нарушение сердечного ритма) впервые обратился в ФГАУ «НМИЦ здоровья детей» Минздрава России с жалобами на периодическую боль в животе и отрыжку. По данным рентгеноконтрастного исследования установлено отсутствие гастроэзофагеального рефлюкса. Выполнена эзофагогастродуоденоскопия (ЭГДС): в верхней и нижней трети пищевода выявлено много участков гетеротопированной слизистой оболочки, максимальный размер которых достигал 3×2 см. Выполнена биопсия нескольких участков гетеротопии. При морфологическом исследовании выявлено, что гетеротопированная ткань соответствует слизистой оболочке желудка. Через 8 месяцев при выполнении контрольной ЭГДС обнаружено, что участки гетеротопии без изменений. В настоящее время пациент получает антирефлюксную и антисекреторную терапию.
Заключение. Гетеротопия слизистой оболочки желудка в пищеводе — частый порок развития. Чаще всего участки эктопии имеют небольшой размер и не дают клинической картины. Однако встречаются «большие участки» гетеротопии, которые могут иметь клинические проявления, такие как боль, изжога и дисфагия. Крупные участки гетеротопии (в нижней трети пищевода) необходимо дифференцировать с пищеводом Баррета. В данном случае не возникло сомнений, что у данного пациента гетеротопия, а не метаплазия слизистой оболочки. Это подтверждено макроскопической картиной («оторванность» от Z-линии, нециркулярное расположение), а также отсутствием гастроэзофагеального рефлюкса по данным рентгеноконтрастного исследования. Следует обратить внимание на то, что у пациентов с гетеротопией слизистой оболочки желудка существует риск малигнизации. Учитывая онконастороженность, необходимо выполнять контрольную эзофагогастродуоденоскопию и оценивать участки гетеротопии в динамике.
Острый некроз слизистой оболочки пищевода или «черный пищевод» — редкое, остро возникающее заболевание, характеризующееся изолированным поражением слизистой оболочки пищевода, клиническими признаками кровотечения в сочетании с тяжелыми метаболическими нарушениями. Диагноз можно установить по данным эндоскопического обследования верхних отделов желудочно-кишечного тракта. В данной статье представлены случаи эндоскопической диагностики данного заболевания у 5 пациентов, которые госпитализированы в клинику с диагнозом желудочно-кишечного кровотечения. При эндоскопическом исследовании выявлен острый некроз слизистой оболочки пищевода, отмечено отсутствие изменений в зоне пищеводно-желудочного перехода. Эрозивно-язвенные изменения желудка и двенадцатиперстной кишки диагностированы у всех пациентов. У 4 пациентов имелась тяжелая сопутствующая патология (артериальная гипертензия, сахарный диабет, ишемическая болезнь сердца). В 80% случаев имело место злоупотребление алкоголем. Во всех случаях пациентам проводилось лечение как основного синдрома (с применением высоких доз ингибиторов протонной помпы), так и сопутствующей патологии. Хороший эффект получен в трех случаях. Двое пациентов скончались на фоне прогрессирования полиорганной недостаточности. Вероятность острого некроза слизистой оболочки пищевода следует учитывать в процессе дифференциальной диагностике при наличии симптомов одинофагии и желудочно-кишечного кровотечения у пациентов, поступающих в стационар.
Цель исследования. Обобщить имеющиеся данные о патогенезе внекишечных проявлений (ВКП) воспалительных заболеваний кишечника (ВЗК) с целью более полного понимания и формирования патогенетической концепции воспалительных заболеваний кишечника и ведения пациентов с данной патологией.
Материал и методы. Проведен поиск статей в базе данных PubMed за период с 1965 по 2021 г. с описанием случаев возникновения ВКП ВЗК, существующих и перспективных методов их лечения. Выполнен литературный обзор.
Результаты. Патогенез развития ВКП является мультифакториальным, он ассоциирован с обеднением кишечной микрофлоры, опосредован выработкой системных аутоантител и связан с повышенным риском развития онкологических заболеваний.
Заключение. Ввиду обширности проявлений воспалительных заболеваний кишечника необходим мультидисциплинарный и индивидуальный подход к ведению пациентов, а также есть основания для дальнейшего изучения концепций развития данной группы заболеваний и их системных проявлений, что, в свою очередь, влияет на подбор и поиск таргетной биологической терапии.
С начала XXI века на фоне промышленной революции в индустрии продуктов питания и напитков наблюдается тенденция к увеличению количества скрытых подсластителей, в основном в виде сахарозы и кукурузного сиропа с высоким содержанием фруктозы. В отличие от глюкозы, метаболизм фруктозы, поступившей с пищей, происходит главным образом в печени, что позволяет считать этот орган и протекающие в нем процессы ключом к пониманию неблагоприятного влияния фруктозы на организм. На сегодняшний день накоплены данные, подтверждающие, что именно фруктоза является фактором, способствующим развитию метаболического синдрома. В настоящем обзоре рассмотрены потенциальные механизмы взаимосвязи избыточного потребления фруктозы и развития ожирения и неалкогольной жировой болезни печени.
Цель обзора. Провести краткий анализ и обсудить основные положения обновленной версии Чикагской классификации нарушений моторной функции пищевода (версия 4.0), опубликованной впервые в 2021 г. в журнале Neurogastroenterology and Motility (Нейрогастроэнтерология и моторика).
Основные положения. Чикагская классификация версия 4.0 представляет собой обновленную классификационную схему нарушений моторики пищевода с использованием показателей манометрии высокого разрешения. Над разработкой новой классификации в течение двух лет работали 7 экспертных групп (52 эксперта в области манометрии пищевода из разных стран). Ключевые обновления Чикагской классификации версии 4.0 включают описание более тщательной и расширенной методики проведения исследования, использование провокационных тестов. В отличие от предыдущей версии, Чикагская классификация версия 4.0 подразумевает обязательное описание исходных манометрических параметров пищеводно-желудочного соединения. Кроме того, внесены обновления и более строгие критерии в диагностику нарушений проходимости пищеводно-желудочного соединения, неэффективной моторики пищевода. В зависимости от наличия и выраженности клинических симптомов, результатов провокационных тестов в новой версии Чикагской классификации допускается выдача заключения после проведения манометрии пищевода как в виде окончательного, так и виде неподтвержденного манометрического диагноза.
Заключение. Основные положения Чикагской классификации нарушений моторики пищевода 4-го пересмотра в целом подтвердили предыдущую версию данного документа. Изменения, внесенные советом экспертов в обновленную версию Чикагской классификации, касались расширенного применения провокационных тестов для обеспечения более точной диагностики заболеваний, сопровождающихся обструкцией нижнего пищеводного сфинктера. Введены новые диагностические критерии для стандартизированной диагностики нарушений моторики пищевода.
Информированное добровольное согласие (ИДС) на проведение эндоскопического вмешательства — это медико-юридический документ, целью которого является урегулирование взаимоотношений между пациентом, врачом и клиникой. Этот документ является информационным, раскрывающим суть вмешательства для пациента, в том числе риски, ассоциированные с вмешательством. Наличие и детализация рисков, связанных с оказанием медицинской помощи, должны быть обязательной составляющей ИДС, о чем говорит Федеральный закон от 21.11.11 №323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации». Отсутствие стандартизованного ИДС по специальности «эндоскопия», отвечающего современным юридическим стандартам, послужило причиной организации серии мероприятий с целью его формирования под эгидой Ассоциации врачей-экспертов качества медицинской помощи. Результатом этого мероприятия явилось создание ИДС по основным направлениям эндоскопии, в том числе по верхним отделам желудочно-кишечного тракта, в котором одной из составляющих является стандартизованная информация о структуре возможных осложнений, связанных как с диагностическим, так и с лечебным вмешательством.
Цель исследования. Изучение причин высокого удельного веса случаев посмертной диагностики гепатоцеллюлярного рака (ГЦР), влияния демографических показателей на вероятность посмертного установления диагноза.
Материал и методы. В ретроспективное наблюдательное исследование включили данные больных ГЦР, жителей Свердловской области, диагноз у которых был установлен в 2015—2021 гг. Оценивали удельный вес случаев посмертной диагностики. Сравнивали показатели больных с прижизненным (325 пациентов) и посмертным диагнозом (351 пациентов). Последние были разделены на две группы: 227 пациентов, которые обращались в течение года до смерти за медицинской помощью, и 124 пациента, которые не обращались.
Результаты. Удельный вес посмертной диагностики ГЦР в течение последних 7 лет составил 46,3%. Вероятность посмертной диагностики была выше в 1,57 раза у больных старше 65 лет (p<0,001), в 1,19 раза — у лиц женского пола (p=0,02), в 2,1 раза — при отсутствии цирроза печени (p<0,001). Место жительства достоверно не влияло на вероятность прижизненной диагностики. Более 60% пациентов с посмертной диагностикой обращались за медицинской помощью в течение года до смерти, и онкологический диагноз у них не был заподозрен. Большинство таких больных получили плановую амбулаторную помощь терапевтического профиля.
Заключение. Большая доля посмертного выявления ГЦР диктует необходимость реализации программ скрининга среди групп риска и повышения онкологической настороженности у врачей общей лечебной сети.
Более чем у 75% пациентов с болезнью Крона в течение жизни возникает потребность как минимум в одном хирургическом вмешательстве по поводу осложнений данного заболевания. В послеоперационном периоде для своевременной активизации и восстановления пациента необходимо адекватное обезболивание. Однако у данных пациентов интенсивность послеоперационного болевого синдрома гораздо выше, чем у пациентов онкологического или общего хирургического профиля, что связано с нерегулируемым воспалением, характерным для болезни Крона.
Цель исследования. Сравнить болевой синдром после илеоцекальной резекции при болезни Крона и правосторонней гемиколэктомии по поводу рака слепой кишки.
Материал и методы. В исследование ретроспективно включены 2 группы пациентов по 22 человека (основная — оперированные по поводу осложнений болезни Крона в объеме лапароскопической илеоцекальной резекции, контрольная — оперированные по поводу рака слепой кишки в объеме лапароскопической правосторонней гемиколэктомии) в период с 2015 по 2021 г. У всех пациентов в раннем послеоперационном периоде выполнена оценка интенсивности болевого синдрома по визуальной аналоговой шкале и уровня C-реактивного белка в крови.
Результаты. Интенсивность болевого синдрома различалась у пациентов основной и контрольной групп статистически значимо в первые 3 суток после операции (p=0,03), статистически незначимо — в последующем (p=0,13). Уровень C-реактивного белка у пациентов основной группы в раннем послеоперационном периоде был выше, чем у пациентов контрольной группы (p<0,05). Опиоидные аналгетики у пациентов с болезнью Крона использовались статистически значимо чаще (p=0,03).
Выводы. У пациентов с болезнью Крона значительно выше болевой синдром и уровень C-реактивного белка в раннем послеоперационном периоде по сравнению с пациентами контрольной группы, также выявлена корреляция между интенсивностью боли и уровнем воспалительных маркеров.
Цель исследования. Изучить уровни интерлейкина-10 (IL-10) у пациентов с гепатитом и циррозом печени алкогольной этиологии.
Материал и методы. Исследование выполнено по протоколу контролируемого исследования методов диагностики случай—контроль. Обследовано 18 пациентов с хроническим гепатитом, 41 пациент с циррозом печени алкогольной этиологии и 15 практически здоровых лиц.
Результаты. Установлено, что уровень IL-10 у пациентов с циррозом печени (3,15; 0,37—9,2 пг/мл) выше, чем у контрольной группы (0; 0—2,7 пг/мл, p<0,01). Уровень IL-10 у пациентов с циррозом печени и пациентов с хроническим гепатитом (0; 0—5,92 пг/мл, p>0,05), как и у пациентов с хроническим гепатитом и контрольной группе статистически не различаются (p>0,05). У пациентов с циррозом печени класса B и C по Child-Puge уровень IL-10 статистически значимо выше (3,15; 1,76—8,24 пг/мл и 6,16; 0,37—12,4 пкг/мл соответственно), чем у пациентов с циррозом печени класса A по Child-Puge (0,37; 0—0,83 пг/мл, p<0,05). У пациентов с прогрессирующими формами цирроза печени (класс B и C) уровень IL-10 статистически значимо выше, чем у пациентов с хроническим гепатитом и циррозом печени класса A (p<0,05). У пациентов с циррозом печени установлены корреляции средней силы IL-10 с уровнем Fib4 (r=0,54), APRI (r=0,58), Forns (r=0,64), эритроцитов (r= –0,6), гемоглобина (r= –0,6), тромбоцитов (r= –0,63), лимфоцитов (r= –0,52), сегментоядерных нейтрофилов (r=0,47), протромбинового индекса (r= –0,59), активированного частичного тромбопластинового времени (r=0,37).
Заключение. Интерлейкин-10, предупреждая процессы воспаления и некроза, а также стимулируя регенеративные процессы, является важным противовоспалительным цитокином, участвующим в патогенезе алкоголь-зависимых заболеваний печени.
Распространенность язвенной болезни среди взрослого населения достигает 10%, причем язвенная болезнь желудка (ЯБЖ) характерна для лиц в возрасте 55—70 лет. ЯБЖ является мультифакториальной патологией, в развитие которой большой вклад вносят наследственные факторы и инфекция H. pylori.
Цель исследования. Изучить роль полиморфных вариантов генов-кандидатов (rs2294008 гена PSCA, rs6136 гена SELP, rs505922, rs8176720, rs2519093, rs507666 гена АВО, rs651007, rs579459, rs649129 гена ABO/RF00019) в развитии H. pyloriпозитивной ЯБЖ.
Материал и методы. В настоящем исследовании участвовали 98 больных H. pylori-позитивной ЯБЖ и 347 индивидуумов контрольной группы, оценка регуляторного потенциала отобранных для изучения SNPs проводилась с помощью интернет-ресурсов HaploReg v4.1, PolyPhen-2, GTEx Portal, генотипирование осуществлено молекулярно-генетическим методом с применением полимеразной цепной реакции. Анализ ассоциаций проведен методом логистической регрессии в рамках аллельной, аддитивной, доминантной и рецессивной генетических моделей.
Результаты. Аллель C гена SELP (rs6136) является генетическим фактором риска развития H. pylori-позитивной ЯБЖ (ОШ=1,66; 95% ДИ 1,02—2,71; p=0,041; pperm=0,042). Полиморфизм rs6136 имеет выраженный регуляторный потенциал, является несинонимичным, рисковый в отношении развития H. pylori-позитивной ЯБЖ аллель C rs6136 ассоциирован с повышенной экспрессией гена F5 и снижением альтернативного сплайсинга гена BLZF1.
Выводы. Генетическим фактором риска развития H. pylori-позитивной язвенной болезни желудка является аллель C гена SELP (rs6136).
Цель исследования. Оценка результатов применения металлических саморасправляющихся стентов у пациентов с дисфагией злокачественного генеза.
Материал и методы. За период 2006—2021 гг. установка металлических саморасправляющихся стентов при злокачественной дисфагии проведена 216 пациентам (средний возраст 62,03±11,61 года; 163 мужчины и 53 женщины). У 111 пациентов был рак пищевода, у 53 — рак кардиального отдела желудка с переходом на пищевод, у 23 — компрессия из-за сдавления извне при других опухолях, у 28 — рецидив рака после операций на пищеводе и желудке, у 1 — нейрофиброматоз легких и средостения.
Результаты. Осложнений при установке стента не было. Осложнения в послеоперационном периоде разделены на ранние (до двух недель после установки) — 12 пациентов (исключая болевой синдром), и поздние (свыше двух недель после установки) — 45 пациентов. Два пациента погибли из-за массивного кровотечения. Большинство осложнений успешно устранены с использованием эндоскопических методов, в том числе путем стентирования по типу «стент в стент», стентирования трахеи из-за прорастания опухоли.
Выводы. Установка стентов у пациентов с дисфагией злокачественного генеза является методом выбора. Стентирование под рентгенологическим контролем может быть применено на этапах освоения метода и при «высокой» локализации проксимального края стеноза. В остальных случаях достаточно эндоскопического контроля. Необходима организация обратной связи врач-пациент или врач-родственник для своевременного выявления и коррекции осложнений. Более 95% осложнений после стентирования могут быть устранены с использованием эндоскопических методов.
Статистика статьи
Статистика просмотров за 2026 год.
Издательство
- Издательство
- МЕДИА СФЕРА
- Регион
- Россия, Москва
- Почтовый адрес
- Издательство «Медиа Сфера», а/я 54, Москва, Россия, 127238
- Юр. адрес
- 127238, город Москва, Дмитровское ш, д. 46 к. 2 стр. 2
- ФИО
- Немцова Нина Валерьевна (ГЕНЕРАЛЬНЫЙ ДИРЕКТОР)
- E-mail адрес
- info@mediasphera.ru
- Контактный телефон
- +7 (495) 4824329