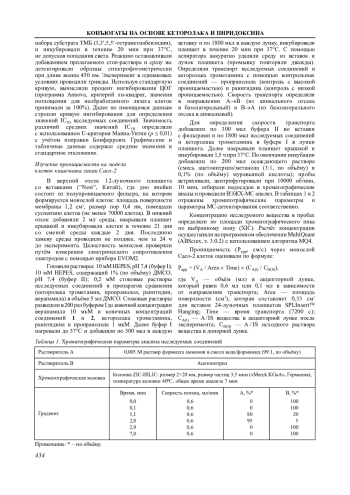
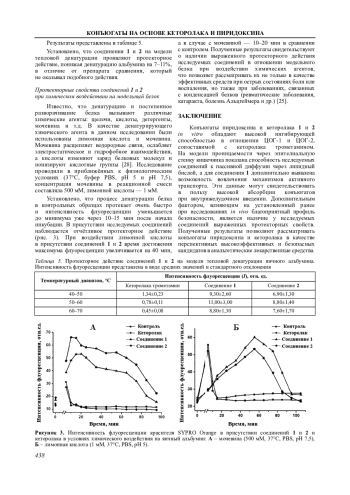
Пролекарственные бифармакофорные конъюгаты на основе пиридоксина и наиболее мощного из всех известных НПВС анальгетика кеторолака in vivo проявляют сопоставимую с кеторолаком анальгетическую активность, но при этом обладают значительно более высокой безопасностью и пролонгированностью действия. В настоящей работе in vitro исследованы антиоксидантные и протекторные свойства двух пролекарственных бифармакофорных конъюгатов на основе пиридоксина и кеторолака, их ингибирующая активность в отношении циклооксигеназы (ЦОГ), а также внутриклеточная проницаемость на модели клеток кишечника линии Сасо-2. Показано, что данные соединения ингибируют ЦОГ-1 и ЦОГ-2 на уровне кеторолака со значениями IC50 в интервале от 12,0 мкМ до 34,7 мкМ. Они оказывают выраженное протекторное действие в условиях теплового и химического воздействия мочевины и лимонной кислоты в отношении альбумина и могут проникать в клетки посредством пассивной диффузии.
Идентификаторы и классификаторы
- SCI
- Химия
Кеторолак — представитель обширной фармакологической группы нестероидных противовоспалительных средств (НПВС), который применяется в основном для кратковременного купирования умеренной и острой боли [1, 2]. В отличие от опиоидных анальгетиков, кеторолак не влияет на опиоидные рецепторы, что исключает характерные для них побочные эффекты — угнетение дыхания и развитие лекарственной зависимости [3, 4]. Фармакологический эффект обусловлен неселективным ингибированием циклооксигеназ (ЦОГ-1 и ЦОГ-2), что приводит к подавлению синтеза простагландинов и, как следствие, ключевых фаз воспаления, обеспечивая высокое анальгезирующее и умеренное противовоспалительное и жаропонижающее действие [5, 6]. Однако применение кеторолака связано с высоким риском развития нежелательных реакций со стороны желудочно-кишечного тракта, сердечно-сосудистой системы, печени и почек, обусловленных неселективным ингибированием ЦОГ и прямым ульцерогенным действием препарата, что ограничивает возможность его длительного применения, в частности, при хронических болевых синдромах [7, 8]. В связи с этим разработка НПВС с улучшенным профилем безопасности и эффективности является одной из ключевых задач современной фармакологии [9].
Если у вас возникли вопросы или появились предложения по содержанию статьи, пожалуйста, направляйте их в рамках данной темы.
Список литературы
1. Каратеев А.Е. (2011) Кеторолак в клинической практике. Неврология, нейропсихиатрия, психосоматика, 3(4), 81-89. DOI: 10.14412/2074-2711-2011-352
Karateev A.E. (2011) Ketorolac in clinical practice. Neurology, Neuropsychiatry, Psychosomatics, 3(4), 81-89.
2. Матвеев А.В., Крашенинников А.Е., Егорова Е.А. (2018) Современный взгляд на эффективность и безопасность кеторолака. РМЖ. Медицинское обозрение, 2(4), 34-39.
Matveev A.V., Krasheninnikov A.E., Egorova E.A. (2018) Modern view on the efficacy and safety of ketorolac. RMJ. Medical Review, 2(4), 34-39.
3. Cepeda M.S., Carr D.B., Miranda N., Diaz A., Silva C., Morales O. (2005) Comparison of morphine, ketorolac, and their combination for postoperative pain: results from a large, randomized, double-blind trial. Anesthesiology, 103(6), 1225-1232. DOI: 10.1097/00000542-200512000-00018
4. Журавлева М.В., Кукес В.Г., Прокофьев А.Б., Сереброва С.Ю., Городецкая Г.И., Бердникова Н.Г. (2016) Рациональное применение НПВП - баланс эффективности и безопасности (обзор литературы). Международный журнал прикладных и фундаментальных исследований, 6(4), 687-696.
Zhuravleva M.V., Kukes V.G., Prokofiev A.B., Serebrova S.Yu., Gorodetskaya G.I., Berdnikova N.G. (2016) Rational use of NSAIDs - balance of efficiency and safety (review). International Journal of Applied and Fundamental Research, 6(4), 687-696.
5. Григорович Р.И., Немахова Е.А., Лаврентьев А.А., Попов П.А. (2010) Нестероидные противовоспалительные средства: анестезиологическая эффективность и основы безопасного применения (обзор литературы). Вестник новых медицинских технологий, 17(2), 175-179.
Grigorovich R.I., Nemakhova E.A., Lavrentiev A.A., Popov P.A. (2010) NAID: anesthesiology effectiveness and basis of safe using (review of literature). Journal of New Medical Technologies, 17(2), 175-179.
6. Каратеев А.Е., Алейникова Т.Л. (2016) Эйкозаноиды и воспаление. Современная ревматология, 10(4), 73-86. DOI: 10.14412/1996-7012-2016-4-73-86
Karateev A.E., Aleynikova T.L. (2016) Eicosanoids and inflammation. Modern Rheumatology Journal, 10(4), 73-86.
7. Drini M. (2017) Peptic ulcer disease and non-steroidal anti-inflammatory drugs. Australian Prescriber, 40(3), 91-93. DOI: 10.18773/austprescr.2017.037
8. Sohail R., Mathew M., Patel K.K., Reddy S.A., Haider Z., Naria M., Habib A., Abdin Z.U., Razzaq Chaudhry W., Akbar A. (2023) Effects of non-steroidal anti-inflammatory drugs (NSAIDs) and gastroprotective NSAIDs on the gastrointestinal tract: a narrative review. Cureus, 15(4), e37080. DOI: 10.7759/cureus.37080
9. Bindu S., Mazumder S., Bandyopadhyay U. (2020) Non-steroidal anti-inflammatory drugs (NSAIDs) and organ damage: a current perspective. Biochem. Pharmacol., 180, 114147. DOI: 10.1016/j.bcp.2020.114147
10. Пугачев М.В., Штырлин Н.В., Агафонова М.Н., Васильева О.С., Фафанова Е.М., Штырлин Ю.Г. (2024) Синтез и анальгетическая активность пролекарственных бифармакофорных производных на основе пиридоксина и кеторолака. Ученые записки Казанского университета. Серия Естественные науки, 166(4), 608-622. DOI: 10.26907/2542-064X.2024.4.608-622
Pugachev M.V., Shtyrlin N.V., Agafonova M.N., Vasileva O.S., Fafanova E.M., Shtyrlin Yu.G. (2024) Synthesis and analgesic properties of prodrug bipharmacophore compounds based on pyridoxine and ketorolac. Uchenye Zapiski Kazanskogo Universiteta Seriya Estestvennye Nauki, 166(4), 608-622.
11. Васильева О.С., Агафонова М.Н., Пугачев М.В., Маланьева А.Г., Штырлин Ю.Г. (2025) Анальгетические и противовоспалительные свойства пролекарственных бифармакофорных производных на основе пиридоксина и кеторолака. Ученые записки Казанского университета. Серия Естественные науки, 167(3), 371-384. DOI: 10.26907/2542-064X.2025.3.371-384
Vasileva O.S., Agafonova M.N., Pugachev M.V., Malanyeva A.G., Shtyrlin Yu.G. (2025) Analgesic and anti-inflammatory properties of bipharmacophore prodrug derivatives based on pyridoxine and ketorolac. Uchenye Zapiski Kazanskogo Universiteta Seriya Estestvennye Nauki, 167(3), 371-384.
12. Lea T. (2015) Caco-2 Cell Line. In: The Impact of Food Bioactives on Health: In Vitro and Ex Vivo Models (Verhoeckx K., Cotter P., López-Expósito I., Kleiveland C., Lea T., Mackie A., Requena T., Swiatecka D., Wichers H., eds.), Cham (CH): Springer. DOI: 10.1007/978-3-319-16104-4_10
13. Chen G., Liu W., Yan B. (2022) Breast cancer MCF-7 cell spheroid culture for drug discovery and development. J. Cancer Ther., 13(3), 117-130. DOI: 10.4236/jct.2022.133009
14. Тельгузиева Ж.А. (2009) Применение ингибиторов ЦОГ-2 в онкологической практике. Медицина и экология, 2(51), 18-22.
Telguziyeva Zh.A. (2009) Application of inhibitors of cyclooxygenase-2 in oncologic practice. Medicine and Ecology, 2(51), 18-22.
15. Курсов С.В., Никонов В.В. (2016) Циклооксигеназа: физиологические эффекты, действие ингибиторов и перспективы дальнейшего использования парацетамола (аналитический обзор). Медицина неотложных состояний, 5(76), 27-35. DOI: 10.22141/2224-0586.5.76.2016.76430
Kursov S.V., Nikonov V.V. (2016) Cyclooxygenase: physiological effects, inhibitors action and perspectives of paracetamol usage (analytical review). Emergency Medicine, 5(76), 27-35.
16. Шостак Н.А., Клименко А.А., Демидова Н.А., Аничков Д.А. (2020) Безопасность селективных нестероидных противовоспалительных препаратов: анализ данных последних лет. Клиницист, 14(1-2), 91-99. DOI: 10.17650/1818-8338-2020-14-1-2-91-99
Shostak N.A., Klimenko A.A., Demidova N.A., Anichkov D.A. (2020) Safety of selective non-steroidal anti-inflammatory drugs: analysis of the last years data. The Clinician, 14(1-2), 91-99.
17. Bermejo M., Avdeef A., Ruiz A., Nalda R., Ruell J.A., Tsinman O., González I., Fernández C., Sánchez G., Garrigues T.M., Merino V. (2004) PAMPA - a drug absorption in vitro model 7. Comparing rat in situ, Caco-2, and PAMPA permeability of fluoroquinolones. Eur. J. Pharm. Sci., 21(4), 429-441. DOI: 10.1016/j.ejps.2003.10.009
18. Sambuy Y., de Angelis I., Ranaldi G., Scarino M.L., Stammati A., Zucco F. (2005) The Caco-2 cell line as a model of the intestinal barrier: Influence of cell and culture-related factors on Caco-2 cell functional characteristics. Cell Biol. Toxicol., 21(1), 1-26. DOI: 10.1007/s10565-005-0085-6
19. Artursson P., Karlsson J. (1991) Correlation between oral drug absorption in humans and apparent drug permeability coefficients in human intestinal epithelial (Caco-2) cells. Biochem. Biophys. Res. Commun., 175(3), 880-885. DOI: 10.1016/0006-291x(91)91647-u
20. Soeters P.B., Wolfe R.R., Shenkin A. (2019) Hypoalbuminemia: pathogenesis and clinical significance. J. Parenter. Enteral Nutr., 43(2), 181-193. DOI: 10.1002/jpen.1451
21. Bourdon E., Blache D. (2001) The importance of proteins in defense against oxidation. Antioxid. Redox Signal., 3(2), 293-311. DOI: 10.1089/152308601300185241
22. Mooney S., Leuendorf J.-E., Hendrickson C., Hellmann H. (2009) Vitamin B6: a long known compound of surprising complexity. Molecules, 14(1), 329-351. DOI: 10.3390/molecules14010329
23. Saso L., Valentini G., Casini M.L., Grippa E., Gatto M.T., Leone M.G., Silvestrini B. (2001) Inhibition of heat-induced denaturation of albumin by nonsteroidal antiinflammatory drugs (NSAIDs): pharmacological implications. Arch. Pharm. Res., 24(2), 150-158. DOI: 10.1007/BF02976483
24. Ziesenitz V.C., Welzel T., van Dyk M., Saur P., Gorenflo M., van den Anker J.N. (2022) Efficacy and safety of NSAIDs in infants: a comprehensive review of the literature of the past 20 years. Pediatric Drugs, 24(6), 603-655. DOI: 10.1007/s40272-022-00514-1
25. Vlad S.C., Miller D.R., Kowall N.W., Felson D.T. (2008) Protective effects of NSAIDs on the development of Alzheimer disease. Neurology, 70(19), 1672-1677. DOI: 10.1212/01.wnl.0000311269.57716.63
26. Космачевская О.В., Насыбуллина Э.И., Шумаев К.Б., Чумикина Л.В., Арабова Л.И., Яглова Н.В., Обернихин С.С., Топунов А.Ф. (2021) Динитрозильные комплексы железа с глутатионовыми лигандами перехватывают пероксинитрит и защищают гемоглобин от окислительной модификации. Прикладная биохимия и микробиология, 57(4), 315-325. DOI: 10.31857/S0555109921040097
Kosmachevskaya O.V., Nasybullina E.I., Shumaev K.B., Chumikina L.V., Arabova L.I., Yaglova N.V., Obernikhin S.S., Topunov A.F. (2021) Dinitrosyl iron complexes with glutathione ligands intercept peroxynitrite and protect hemoglobin from oxidative modification. Appl. Biochem. Microbiol., 57(4), 411-420. DOI: 10.1134/S0003683821040098
27. Mahran R., Vello N., Komulainen A., Malakoutikhah M., Härmä H., Kopra K. (2023) Isothermal chemical denaturation assay for monitoring protein stability and inhibitor interactions. Sci. Rep., 13, 20066. DOI: 10.1038/s41598-023-46720-w
28. Bennion B.J., Daggett V. (2003) The molecular basis for the chemical denaturation of proteins by urea. Proc. Natl. Acad. Sci. USA, 100(9), 5142-5147.
Выпуск
Другие статьи выпуска
Использование in silico подходов для оценки потенциальных нежелательных реакций новых фармацевтических субстанций позволяет уменьшить риски, а также финансовые и временные затраты, связанные с разработкой лекарственных средств. С помощью разработанного нами ранее метода выявления химических мотивов, ассоциированных с определёнными типами нежелательной биологической активности, мы оценили “off-target” токсичность клинически исследуемых фармацевтических субстанций, чтобы оценить потенциальные риски их дальнейшего исследования и использования в клинической практике. Для этого созданы структурные фрагменты, высокоспецифичные для ингибиторов рецептора эпидермального фактора роста и дипептидилпептидазы 4 — двух молекулярных мишеней, ассоциированных с широким спектром нежелательных реакций. Проведён поиск соединений, содержащих созданные фрагменты, среди 12070 записей базы данных PubChem, содержащих информацию о проведении клинических испытаний. Показано, что пять соединений, исследуемых в фазах I и II, могут обладать неблагоприятным соотношением “польза-риск”, возникающим из-за потенциального ингибирования одного из двух анализируемых ферментов. Применение подобных аналитических стратегий на ранних доклинических этапах разработки может значительно снизить совокупные финансовые и временные затраты, способствуя ускоренному выводу на рынок более безопасных и доступных лекарственных средств.
Сепсис-ассоциированная энцефалопатия (САЭ) представляет собой острую дисфункцию головного мозга, которая возникает при отсутствии первичного очага инфекции в центральной нервной системе. Целью нашей работы было проведение пилотного нецелевого метаболомного исследования плазмы крови пациентов с САЭ для выявления метаболических изменений, потенциально связанных с патологическим состоянием, и формирования гипотез для дальнейшего изучения патогенеза, поиска перспективных биомаркеров и оценки тяжести состояния септического пациента. Метаболомное профилирование осуществлялось методом ВЭЖХ-МС-ВР с последующим статистическим анализом полученных данных. В результате слепого рандомизированного контролируемого клинического исследования выявлено существенное различие в метаболических профилях основной и контрольной групп. Функциональный анализ позволил обнаружить метаболические пути, наиболее затронутые патологическими процессами у пациентов с САЭ: метаболизм ацилкарнитинов, лизофосфатидилхолинов, таурина, биосинтез фолата и метаболизм лекарственных препаратов — субстрата цитохрома Р450. У больных с САЭ с нарушением сознания в виде делирия и комы отмечено снижение уровня длинноцепочечных ацилкарнитинов и содержания лизофосфатидилхолинов. Метаболомные профили пациентов с САЭ значимо различались в группе умерших и выживших пациентов: концентрации серосодержащих аминокислот в группе умерших были значительно ниже, чем в группе выживших. В нашем исследовании установлены 64 кандидата в биомаркеры, которые потенциально могут быть использованы для прогнозирования исходов сепсиса, что требует дальнейшего изучения с использованием расширенной и независимой когорты пациентов.
Ионы меди (Cu2+) в концентрации 25–50 мкМ стимулируют вызванную липополисахаридом (ЛПС) продукцию оксида азота (NO) в культурах глиальных клеток, полученных из коры головного мозга крыс и содержащих как астроциты, так и клетки микроглии. Более высокая концентрация Cu2+ (100 мкМ) при стимуляции ЛПС не вызывала достоверного повышения NO в среде инкубации, а при 200 мкМ Cu2+ происходило снижение этого параметра по сравнению с ЛПС. Ионы Cu2+ в этих концентрациях снижали жизнеспособность культивируемых клеток. Видимо, снижение жизнеспособности клеток не связано с накоплением нитритов, так как добавление в среду культивирования даже 100 мкМ нитрита натрия не снижало выживаемость клеток и не влияло на цитотоксичность Cu2+. Исследование клеток микроглии (маркер IBA1) показало, что в культурах, обработанных ЛПС, микроглия имела преимущественно распластанную амебоидную морфологию, характерную для активированной микроглии. Кроме того, под действием ЛПС происходило увеличение площади профильного поля тела клеток и периметра. В концентрации 25 мкМ ионы Cu2+ не влияли на морфологические изменения клеток микроглии, связанные с воспалительным фенотипом. Нельзя исключать, что усиление ионами меди продукции NO, вызванной ЛПС, опосредовано астроцитами.
Фактор некроза опухоли-α (TNFα) — ключевой провоспалительный цитокин, повышение уровня которого наблюдается при воспалительных заболеваниях верхних дыхательных путей. В работе исследовано дозо- и времязависимое влияние TNFα (1–100 нг/мл, 6–48 ч) на линию клеток RPMI 2650 — модели назального эпителия. Кратковременное воздействие (6 ч) вызывало активацию NF-κB и повышение уровня белков межклеточных контактов E-кадгерина и ZO-1 без существенного влияния на жизнеспособность. Продолжительная экспозиция (24–48 ч) приводила к увеличению уровня про-IL-1β, активации апоптоза и снижению жизнеспособности клеток. При этом отмечалось снижение уровня белков межклеточных контактов. Таким образом, при кратковременном воздействии TNFα может оказывать защитное действие, повышая плотность межклеточных контактов, а при увеличении длительности экспозиции он запускает процессы апоптоза и снижает плотность межклеточных контактов, что может способствовать повышению проницаемости клеточного слоя.
Мультиформная глиобластома (ГБМ) — наиболее агрессивная первичная опухоль головного мозга, характеризующаяся крайне неблагоприятным прогнозом. Трудности в диагностике и мониторинге данного заболевания создают необходимость поиска минимально инвазивных подходов, среди которых перспективным направлением считается жидкостная биопсия. Данный обзор посвящен анализу результатов современных исследований, направленных на поиск циркулирующих белковых биомаркеров ГБМ в плазме и сыворотке крови. В качестве биомаркеров рассматриваются свободно циркулирующие белки плазмы крови и белки, находящиеся в составе внеклеточных везикул (ВнВ). В обзоре обобщены результаты работ, использующих для поиска белковых биомаркеров как иммунохимические методы, так и масс-спектрометрические подходы, а также представлен перечень выявленных потенциальных диагностических и прогностических биомаркеров. Анализ представленных в литературе работ показывает, что протеомный анализ, сосредоточенный на фракции ВнВ плазмы крови, существенно расширяет возможности поиска биомаркеров для неинвазивной диагностики и мониторинга ГБМ.
Эпидемиологические исследования показывают, что во всём мире, в том числе в РФ, наблюдается устойчивый рост числа пациентов с когнитивными нарушениями, связанными с нейродегенеративными заболеваниями и различными аффективными расстройствами. В связи с этим существует запрос на разработку более действенных терапевтических подходов к их коррекции. Установлено, что регулярная физическая нагрузка способствует улучшению когнитивных функций и подавляет симптомы депрессии. Работающие мышцы секретируют биологически активные вещества — миокины, регулирующие восстановление самих мышц, а также регулирующие функции внутренних органов, желёз внутренней секреции, иммунной системы и мозга. Результатом является скоординированный ответ органов и систем, направленный на восстановление функциональной активности организма после физической нагрузки. В частности, улучшается память и способность к обучению. Пациенты с когнитивными нарушениями или депрессией часто не способны вовлечься в регулярную физическую активность из-за физических ограничений или ослабления мотивации. В связи с этим фармацевтические препараты, имитирующие эффекты мышечной активности, являются перспективной терапевтической опцией. Одним из направлений может стать создание препаратов на основе миокина иризина, который вырабатывается во время физической нагрузки и оказывает целый ряд благотворных эффектов на когнитивные функции и настроение. В этом обзоре представлены данные по влиянию физической нагрузки на когнитивные функции в норме и при патологии, описано физиологическое действие иризина, представлены предполагаемые механизмы действия иризина на когнитивные функции и симптомы депрессии.
Статистика статьи
Статистика просмотров за 2026 год.
Издательство
- Издательство
- ИБМХ
- Регион
- Россия, Москва
- Почтовый адрес
- 119121, Россия, г. Москва, ул. Погодинская, д. 10, стр.8
- Юр. адрес
- 119121, Россия, г. Москва, ул. Погодинская, д. 10, стр.8
- ФИО
- Пономаренко Елена Александровна (Директор)
- E-mail адрес
- dir@ibmc.msk.ru
- Контактный телефон
- +7 (499) 2466980