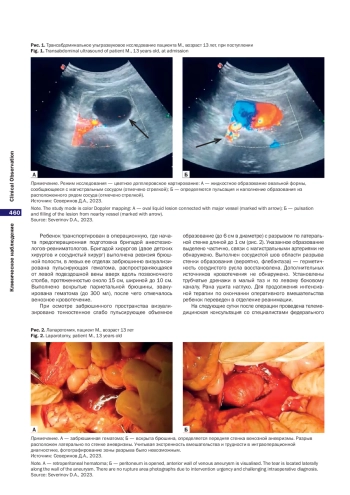
Обоснование. Формирование венозных мальформаций объясняется сохранением первичных венозных систем, образующих в эмбриональный период нижнюю полую вену. Аномалии ее развития приводят к тонкостенной флебэктатической трансформации гонадных вен, травма которых может привести к разрыву с продолжающимся кровотечением. Такие состояния угрожают жизни пациентов при ранее не диагностированных пороках развития сосудистой системы. Описание клинического случая. В приемное отделение бригадой скорой медицинской помощи доставлен мальчик, возраст 13 лет, с жалобами на выраженные боли в левой половине живота и общую слабость. Из анамнеза известно, что за час до обращения ребенок получил удар в живот на тренировке. Общее состояние пациента на момент поступления тяжелое. Отмечаются признаки продолжающегося внутреннего кровотечения по данным ультразвукового исследования брюшной полости и малого таза, падение артериального давления и концентрации гемоглобина. В экстренном порядке проведена срединная лапаротомия, визуализирована забрюшинная гематома больших размеров от подвздошных сосудов слева вверх вдоль позвоночного столба. Во время ревизии забрюшинного пространства после эвакуации гематомы обнаружено тонкостенное образование с частичным разрывом по латеральной стенке. Целостность сосудистой стенки восстановлена. После операции ребенок консультирован специалистами федерального центра по детской сосудистой хирургии, в котором в последующем мальчику проведено реконструктивное вмешательство на сосудах забрюшинного пространства слева — пересечены притоки аневризматично расширенной левой яичковой вены, выполнявшей функцию нижней полой вены у пациента, проведено удаление флебэктатической левой гонадной вены. Ребенок выписан на 10-е сут после операции. Заключение. Врожденные сосудистые аномалии в сочетании с аневризматическими трансформациями являются крайне редким вариантом пороков развития кровеносной системы у детей. Зачастую такие аномалии обнаруживают случайно. По нашему мнению, при обнаружении флебэктатической трансформации эффективна «агрессивная» хирургическая тактика с удалением флебэктазированного участка для профилактики его разрыва и тромбоза.
Предпросмотр статьи
Идентификаторы и классификаторы
Если у вас возникли вопросы или появились предложения по содержанию статьи, пожалуйста, направляйте их в рамках данной темы.