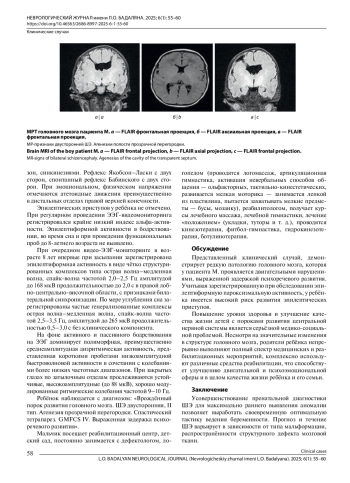
Представлены данные об эпидемиологии, этиологии, патогенезе развития шизэнцефалии, современных методах диагностики и собственное клиническое наблюдение пациента с врождённой шизэнцефалией.
Особенностью клинического случая является редкость данного порока головного мозга, относящегося к корковым дизгенезиям. Длительный катамнез наблюдения отражает особенности развития моторных навыков, речи при отсутствии эпилептических приступов, что крайне редко при обсуждаемой патологии и расширяет комплекс реабилитационных мероприятий, направленных на улучшение качества жизни пациента.
Идентификаторы и классификаторы
Структурные аномалии головного мозга являются актуальной проблемой современной неврологии детского возраста.
Если у вас возникли вопросы или появились предложения по содержанию статьи, пожалуйста, направляйте их в рамках данной темы.
Список литературы
1. Милованова О.А. Корковые дисгенезии, сопровождающиеся эпилептическими синдромами и симптоматической эпилепсией у детей. Журнал неврологии и психиатрии им. С.С. Корсакова. 2015; 115(12): 154-61. DOI: 10.17116/jnevro2015115112154-161
2. Barkovich A.J., Norman D. MR imaging of schizencephaly. AJR Am. J. Roentgenol. 1988; 150(6): 1391-6. DOI: 10.2214/ajr.150.6.1391
3. Yakovlev P.I., Wadsworth R.C. Schizencephalies; a study of the congenital clefts in the cerebral mantle; clefts with fused lips. J. Neuropathol. Exp. Neurol. 1946; 5: 116-30. DOI: 10.1097/00005072-194604000-00003
4. Kamble V., Lahoti A.M., Dhok A., Taori A., Pajnigara N.J A rare case of schizencephaly in an adult with late presentation. J. Family Med. Prim. Care. 2017; 6(2): 450-2. DOI: 10.4103/jfmpc.jfmpc_43_17
5. Гузева В.И., Охрим И.В., Гузева О.В., Гузева В.В., Касумов В.Р. Клинико-функциональные нарушения у пациентов с эпилепсией при шизэнцефалии. Журнал неврологии и психиатрии им. С.С. Корсакова. 2023; 123(3): 46-50. DOI: 10.17116/jnevro202312303146
6. Iannetti P., Nigro G., Spalice A., Faiella A., Boncinelli E. Cytomegalovirus infection and schizencephaly: case reports. Ann. Neurol. 1998; 43(1): 123-7. DOI: 10.1002/ana.410430122
7. Govaert P. Prenatal stroke. Semin. Fetal Neonatal Med. 2009; 14(5): 250-66. DOI: 10.1016/j.siny.2009.07.008
8. Niwa T., Aida N., Osaka H., Wada T., Saitsu H., Imai Y.Intracranial hemorrhage and tortuosity of veins detected on susceptibility-weighted imaging of a child with a type IV collagen α1 mutation and schizencephaly. Magn. Reson. Med. Sci. 2015; 14(3): 223-6. DOI: 10.2463/mrms.2014-0060
9. Sato Y., Shibasaki J., Aida N., Hiiragi K., Kimura Y., Akahira-Azuma M., et al. Novel COL4A1 mutation in a fetus with early prenatal onset of schizencephaly. Hum. Genome Var. 2018; 5: 4. DOI: 10.1038/s41439-018-0005-y
10. Brunelli S., Faiella A., Capra V., Nigro V., Simeone A., Cama A., et al. Germline mutations in the homeobox gene EMX2 in patients with severe schizencephaly. Nat. Genet. 1996; 12(1): 94-6. DOI: 10.1038/ng0196-94
11. Hehr U., Pineda-Alvarez D.E., Uyanik G., Hu P., Zhou N., Hehr A., et al. Heterozygous mutations in SIX3 and SHH are associated with schizencephaly and further expand the clinical spectrum of holoprosencephaly. Hum. Genet. 2010; 127(5): 555-61. DOI: 10.1007/s00439-010-0797-4
12. Chhetri P.K., Raut S. Schizencephaly - A case report. J. Coll. Med. Sci-Nepal. 2010; 6(1): 54-6. DOI: 10.3126/jcmsn.v6i1.3604
13. Choayb S., Chalh O., Allali N., Chat L., Elhaddad S. Unilateral closed-lip schizencephaly.Int. J. Clin. Med. Imaging. 2021; 8(1): 728.
14. Griffiths P.D. Schizencephaly revisited. Neuroradiology. 2018; 60(9): 945-60. DOI: 10.1007/s00234-018-2056-7
15. Трепилец В.М., Хачатрян Л.Г., Быкова О.В. Особенности клинического течения симптоматической фокальной эпилепсии у детей с гемипаретической формой ДЦП. Лечащий врач. 2018; (4): 62-7.
16. Жихарева В.В., Узакбаев К.А., Саатова Г.М., Бабаджанов Н.Д. Медицинская реабилитация детей раннего возраста с неврологическими проявлениями и последствиями врожденных пороков развития нервной системы. Бюллетень науки и практики. 2021; 7(9): 405-9. DOI: 10.33619/2414-2948/70/37
17. Aronica E., Becker A.J., Spreafico R. Malformations of cortical development. Brain Pathol. 2012; 22(3): 380-401. DOI: 10.1111/j.1750-3639.2012.00581.x
18. Klingensmith W.C., Coiffi-Ragan D.T. Schizencephaly: Diagnosis and progression in utero. Radiology. 1986; 159(3): 617-8. DOI: 10.1148/radiology.159.3.3517949
19. Kamble V., Lahoti A.M., Dhok A., Taori A., Pajnigara N. A rare case of schizencephaly in an adult with late presentation. J. Family Med. Prim. Care. 2017; 6(2): 450-2. DOI: 10.4103/jfmpc.jfmpc_43_17
20. Fernández-Mayoralas D.M., Fernández-Jaén A., Jiménez-De-la-Peña M., Recio-Rodríguez M., Muñoz-Jareño N., Arroyo-González R. Schizencephaly: pre- and postnatal magnetic resonance imaging. J. Child Neurol. 2010; 25(8): 1020-3. DOI: 10.1177/0883073809355821
21. Жихарева В.В., Узакбаев К.А., Саатова Г.М., Бабаджанов Н.Д. Медицинская реабилитация детей раннего возраста с неврологическими проявлениями и последствиями врожденных пороков развития нервной системы. Бюллетень науки и практики. 2021; 7(9): 405-9. DOI: 10.33619/2414-2948/70/37
22. Zhang J., Yang Z., Yang Z., He X., Hou Y., Wang Y. Successful surgery for refractory seizures associated with bilateral schizencephaly: two case reports and literature review. Neurol. Sci. 2016; 37(7): 1079-88.
Выпуск
Другие статьи выпуска
Цель обзора — рассмотрение патогенеза, диагностики и методов лечения периферической нейропатии (ПН) при ревматоидном артрите (РА).
ПН является распространённым осложнением РА, значительно ухудшающим качество жизни пациентов и приводящим к инвалидизации. В статье представлен обзор современных данных о патогенезе, клинических проявлениях, диагностике и лечении ПН при РА. В патогенезе ПН участвуют механизмы, включая васкулит, аутоиммунные реакции, нейрогенное воспаление и компрессию нервов. Клинические проявления ПН разнообразны и включают сенсорные, моторные и вегетативные нарушения. Для диагностики используются клинический осмотр, электронейромиография, ультразвуковое исследование, магнитно-резонансная томография (МРТ) и биопсия нерва. МРТ, включая магнитно-резонансную нейрографию, функциональную МРТ и МРТ-спектроскопию, позволяет визуализировать поражённые нервы, оценить их структуру и функцию, выявить изменения в головном мозге, связанные с болью. Лечение ПН при РА включает контроль основного заболевания с помощью базисных противоревматических препаратов и биологической терапии, а также симптоматическое лечение неврологических проявлений. В случаях васкулитной нейропатии может потребоваться более агрессивная терапия с применением высоких доз глюкокортикоидов и/или цитотоксических препаратов. Для лечения компрессионных нейропатий используются консервативные методы и хирургическое вмешательство. Дополнительная терапия включает препараты, влияющие на нейротрансмиттеры, витамины группы В и α-липоевую кислоту. В последние годы появились данные об эффективности палмитоилэтаноламида и птеростильбена в лечении ПН при РА, однако необходимы дальнейшие исследования для подтверждения их эффективности и безопасности. Несмотря на достигнутый прогресс в понимании ПН при РА, остаются вопросы, требующие дальнейшего изучения, включая разработку более эффективных методов лечения и выявление предикторов развития нейропатии.
Цель статьи — представить актуальный и современный обзор парасомний в детском возрасте и способы их фармакологической коррекции. Непреднамеренные двигательные явления у детей делятся на три основные группы: расстройства пробуждения; парасомнии, связанные с фазой быстрого сна; другие виды парасомний. Учёные рассматривают данную проблему многогранно, включая изучение модифицированных триггеров. Детально описаны виды патогенеза быстрого и медленного сна, виды парасомний при данных фазах. При постановке диагноза и диагностике необходимо учитывать анамнез и выявлять триггеры, и в этом объективная роль отводится видеополисомнографии. Следует обратить внимание на фармакологическую коррекцию парасомний, при которой назначаются препараты различных групп (антидепрессанты, транквилизаторы, анксиолитики, адаптогены), однако врачам, которые сталкиваются с данной проблемой, крайне важно понимать их природу и уметь проводить дифференциальную диагностику.
Определение уровней нейрофиламентов (НФ) в сыворотке крови детей с СМА может являться биомаркером тяжести и течения заболевания, а также способом оценки эффективности проведённой патогенетической терапии.
Цель исследования — определить уровни НФ в сыворотке крови детей в возрасте 0–24 мес с СМА I типа и на пресимптоматической стадии заболевания до и после проведения генной терапии препаратом онасемноген абепарвовек (ОА).
Материалы и методы. В исследование были включены 155 детей в возрасте 0–24 мес — 76 неврологически здоровых детей (группа II), а также 79 пациентов с СМА из группы I: подгруппа Ia — 44 ребёнка с СМА I типа, Ib — 35 детей на пресимптоматической стадии заболевания. У большинства детей с подгруппы Ia (n = 43; 97,7%) было 2 копии гена SMN2, в то время как у детей подгруппы Ib (n = 31; 88,6%) — 3 копии.
Результаты. Получены значения лёгких и тяжёлых цепей НФ у детей из группы I до и через 3–6, 7–12 и 13–24 мес после проведения генной терапии ОА. Уровень лёгких цепей НФ в подгруппе Ia до лечения был достоверно выше, чем в подгруппе Ib (p < 0,001) и в группе контроля (p < 0,001). Уровень тяжёлых цепей НФ в подгруппе Ia до лечения был достоверно выше, чем в группе контроля. В подгруппе Ia отмечено достоверное (р < 0,01) снижение уровней лёгких цепей НФ в сыворотке крови через 3–6 мес после проведения генной терапии (Ме [Q1; Q3] — 22,97 [6,00; 48,54]) по сравнению с показателями до лечения (6,0 [5,92; 7,78]). Через 7–12 мес (6,15 [5,15– 7,30]) и 13–24 мес (6,0 [5,7–6,6]) отмечена стабилизация показателей медианы с уменьшением интерквартильных размахов. В подгруппе Ib также отмечено достоверное (р < 0,01) снижение уровней лёгких цепей НФ в сыворотке крови через 3–6 мес после проведения генной терапии ОА (6,0 [6,00; 7,25]) по сравнению с показателями до лечения (6,0 [6,00; 31,43]).
Заключение. Определение уровней лёгких и тяжёлых цепей НФ в сыворотке крови у пациентов с СМА до и после проведения генной терапии ОА может расцениваться как маркер тяжести заболевания и эффективности лечения.
Появление патогенетической терапии значительно изменило прогнозы при спинальной мышечной атрофии (СМА). Однако наши знания о патогенетических методах лечения СМА в значительной степени базируются на результатах клинических исследований, которые во многом ограничены из-за узких критериев отбора пациентов и небольшой продолжительности наблюдения.
Цель исследования — оценить эффективность генной терапии препаратом онасемноген абепарвовек (ОА) у пациентов с СМА I типа с клиническими проявлениями болезни и у детей, находящихся в пресимптоматической стадии заболевания, в рамках реальной клинической практики.
Материалы и методы. В исследование были включены 79 детей со СМА, из них 42 (53,2%) мальчика. Диагноз был верифицирован при проведении молекулярно-генетического исследования. Дети были распределены на две группы в зависимости от наличия или отсутствия у них симптомов СМА на момент включения в исследование: 44 ребёнка имели СМА I типа с дебютом клинических симптомов в возрасте до 6 мес; 35 детей находились на пресимптоматической стадии заболевания. Все пациенты получили ОА, средний возраст на момент проведения генной терапии составил 2,90 ± 1,74 мес (95% ДИ 2,51–3,29), min — 1,00, max — 7,00. Комплексная оценка клинических показателей (этапы двигательного развития по рекомендациям ВОЗ, шкалы HINE-2 и CHOP-INTEND) осуществлялась до инициации генной терапии и через 6, 12, 18 и 24 мес после её проведения.
Результаты. Дети с СМА I типа после проведения генной терапии демонстрировали положительную динамику в двигательном развитии. К концу 2-го года наблюдения хорошо удерживали голову и переворачивались из положения лёжа на спине на живот 88,6% пациентов; сидели без опоры — 60,5%, но только 10,3% смогли сформировать все двигательные навыки, однако ни один из этих детей не сформировал их в соответствии с критериями ВОЗ. Оценка по шкале HINE-2 увеличилась с Ме 2,0 (1,00–2,25) баллов при инициации терапии до 20,00 (16,50–24,50) баллов к концу периода наблюдения. Максимального значения 26 баллов достигли только 2 (4,5%) детей этой группы. Оценка по шкале CHOP-INTEND возросла с Ме 30,0 (22,00–37,25) баллов перед началом лечения до Ме 60,0 (58,0–64,0) баллов к 24 мес наблюдения. Только 11,4% пациентов с СМА I типа достигли максимального значения 64 балла. Большинство пресимптоматических пациентов в нашем исследовании на фоне генной терапии достигли всех двигательных навыков по критериям ВОЗ соответственно своему возрасту. Все дети из этой группы, которые находились под достаточным наблюдением и достигли возраста самостоятельного хождения (23 ребёнка), имели максимальное значение 26 баллов по шкале HINE-2 к возрасту 18 мес. Все дети из этой группы достигли максимального значения по шкале CHOP-INTEND 64 балла к возрасту 6 мес.
Заключение. Применение ОА у детей с СМА I типа существенно модифицирует течение заболевания и значимо улучшает исходы по сравнению с естественной историей развития СМА с дебютом в раннем возрасте, а у большинства пресимптоматических пациентов использование генной терапии приводит к достижению этапов двигательного развития в соответствии с критериями ВОЗ.
Магнитно-резонансная томография (МРТ), в частности функциональная, является одним из наиболее информативных неинвазивных методов определения структурно-функционального состояния головного мозга, и очевидное направление её развития — изучение возможностей данного подхода в различных областях медицины, в том числе в детской неврологии и офтальмологии.
Цель работы — определение показателей межполушарной асимметрии по структурным и функциональным показателям и выявление корреляций этих показателей между собой, а также с клиническим характеристиками у детей с левосторонней амблиопией.
Материалы и методы. В группу для проведения МРТ были включены 20 пациентов с левосторонней амблиопией, однако по итогам проверки качества изображений анализируемая выборка для структурной МРТ составила 17 человек (возраст 6,2–15,1 года; средний возраст 9,5 ± 2,5 года; 9 мальчиков и 8 девочек), для функциональной МРТ покоя — 14 человек (возраст 6,2–15,1 года; средний возраст 9,5 ± 2,5 года; 8 мальчиков и 6 девочек).
Результаты. Выявлены значимые показатели асимметрии для толщины серого вещества в латеральной затылочной коре, объёма таламуса, показателя локальной согласованности гемодинамического сигнала в нижней латеральной затылочной коре, первичной и вторичной зрительной коре, язычной извилине, хотя эти данные не коррелировали с остротой зрения в глазу с амблиопией.
Заключение. Полученные результаты могут быть связаны с изменением нейроонтогенеза, но для подтверждения этого требуются дальнейшие исследования.
Статистика статьи
Статистика просмотров за 2026 год.
Издательство
- Издательство
- НМИЦ здоровья детей
- Регион
- Россия, Москва
- Почтовый адрес
- 119991, город Москва, Ломоносовский пр-кт, д.2 стр.1
- Юр. адрес
- 119991, город Москва, Ломоносовский пр-кт, д.2 стр.1
- ФИО
- Фисенко Андрей Петрович (ДИРЕКТОР)
- E-mail адрес
- director@nczd.ru
- Контактный телефон
- +7 (499) 1343083
- Сайт
- https://nczd.ru