Цель работы. Провести сравнительное изучение болевой чувствительности в тесте hot-plate у самцов и самок крыс, проживавших в условиях социальной изоляции в течение года.
Материал и методы. Работа проведена на 69 крысах Wistar под контролем этического комитета ФГБНУ «НИИОПП». После отсаживания крысят от матери на 29-й постнатальный день их распределяли в 4 группы: социально изолированные самки (n=17) и самцы (n=18), которых содержали поодиночке в течение всего эксперимента, контрольные самки (n=17) и самцы (n=17), которых содержали по 4—5 особей в клетке. Пороги болевых реакций (ПБР) оценивали в тесте hot-plate при t=55±0,3°C по латентному периоду появления избавляющих реакций облизывания передней лапки, задней лапки и прыжка. Тестирование половины крыс проводили в возрасте 10,5 мес, всех крыс — в возрасте 12,5 мес. Статистическую обработку результатов проводили с использованием Factorial и Repeated Measures ANOVA.
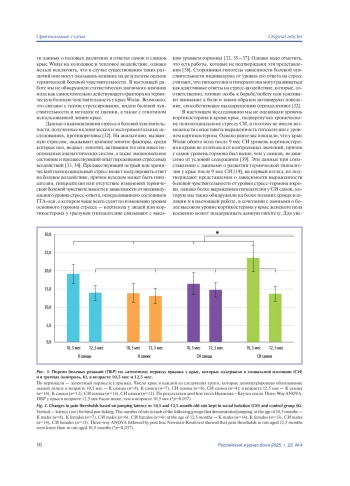
Результаты. Выявлено повышение ПБР у социально изолированных крыс по сравнению с крысами, которых содержали в группах, по увеличению латентного периода облизывания передней лапки (F(1,62)=11,517, p=0,001) и задней лапки (F(1,60)=5,005, p=0,029). У социально изолированных самок и у самцов контрольной группы ПБР облизывания задней лапки были выше, чем у самок контрольной группы. ПБР облизывания задней лапки и прыжка снижались с увеличением возраста у крыс обоего пола, независимо от условий содержания.
Заключение. Повышение ПБР в тесте hot-plate у крыс обоего пола на поздних сроках социальной изоляции в случае ее раннего начала свидетельствует о развитии гипоалгезии, возможно связанной с процессами адаптации к длительному психосоциальному стрессу. Снижение термической болевой чувствительности было более выраженным у самок, чем у самцов.
Идентификаторы и классификаторы
- SCI
- Здравоохранение
Социальная изоляция (СИ) — это один из видов хронического психосоциального стресса. СИ может приводить к тяжелым последствиям — развитию психоэмоциональных, когнитивных и психосоматических нарушений у млекопитающих, проживающих в социальных группах, особенно в случае ее раннего начала [1—4]. Эти изменения, по современным представлениям, обусловлены нейропластическими процессами [5—7]. Прямых свидетельств изменений соматической болевой чувствительности у людей под влиянием длительной СИ в научной литературе найти не удалось, но есть данные, полученные путем телефонного опроса, проведенного после 2—4 мес ограничений социального взаимодействия, вызванных карантином в связи с пандемией COVID-19, о том, что под влиянием СИ ощущение хронической боли в основном усиливалось [8]. Напротив, в единственной работе по результатам телефонного интервью удалось обнаружить улучшение течения мигрени по показателям частоты и интенсивности приступов после двух месяцев карантина в связи с пандемией COVID-19 [9]. На основании этих данных можно с осторожностью предположить, что социальные ограничения в человеческой популяции изменяют не только болевые ощущения, но и болевую чувствительность.
Если у вас возникли вопросы или появились предложения по содержанию статьи, пожалуйста, направляйте их в рамках данной темы.
Список литературы
1. Крупина Н.А., Ширенова С.Д. Нарушения когнитивных функций при длительной социальной изоляции: результаты исследований на людях и экспериментов на животных. Успехи физиологических наук. 2023;54(4):18-35. DOI: 10.1007/s11055-024-01655-1
10.31857/S0301179823040045. DOI: 10.1007/s11055-024-01655-1
2. Patrono A, Renzetti S, Guerini C, Macgowan M, Moncada SM, Placidi D, Memo M, Lucchini RG. Social isolation consequences: lessons from COVID-19 pandemic in a context of dynamic lock-down in Chile. BMC Public Health. 2024 Feb 24;24(1):599. DOI: 10.1186/s12889-024-18064-1
3. Lüönd AM, Wolfensberger L, Wingenbach TSH, Schnyder U, Weilenmann S, Pfaltz MC. Don’t get too close to me: depressed and non-depressed survivors of child maltreatment prefer larger comfortable interpersonal distances towards strangers. Eur J Psychotraumatol. 2022 May 30;13(1):2066457. DOI: 10.1080/20008198.2022.2066457
4. Huang F, Liu X, Guo Q, Mahaman YAR, Zhang B, Wang JZ, Luo H, Liu R, Wang X. Social isolation impairs cognition via Aβ-mediated synaptic dysfunction. Transl Psychiatry. 2024 Sept 18;14(1):380. DOI: 10.1038/s41398-024-03078-5
5. Ширенова С.Д., Хлебникова Н.Н., Крупина Н.А. Длительная социальная изоляция приводит к снижению экспрессии предшественника BDNF и пролилэндопептидазы в структурах мозга крыс. Биохимия. 2021;86(6):857-870. DOI: 10.1134/S0006297921060080
10.31857/S0320972521060087. DOI: 10.1134/S0006297921060080
6. Begni V, Sanson A, Pfeiffer N, Brandwein C, Inta D, Talbot SR, Riva MA, Gass P, Mallien AS. Social isolation in rats: Effects on animal welfare and molecular markers for neuroplasticity. PLoS One. 2020 Oct 27; 15(10):e0240439. Erratum in: PLoS One. 2021 Feb 26;16(2):e0248070. DOI: 10.1371/journal.pone.0248070
7. Geng S, Zhang Z, Liu X, Sun H, Xu T, Sun C, Hu S, Liu A, Yang Z, Xie W, Mu M. Intermittent social isolation enhances social investigation but impairs social memory in adult male mice. Physiol Behav. 2025 Mar 15;291:114788. DOI: 10.1016/j.physbeh.2024.114788
8. García-Esquinas E, Ortolá R, Gine-Vázquez I, Carnicero JA, Mañas A, Lara E, Alvarez-Bustos A, Vicente-Rodriguez G, Sotos-Prieto M, Olaya B, Garcia-Garcia FJ, Gusi N, Banegas JR, Rodríguez-Gómez I, Struijk EA, Martínez-Gómez D, Lana A, Haro JM, Ayuso-Mateos JL, Rodríguez-Mañas L, Ara I, Miret M, Rodríguez-Artalejo F. Changes in Health Behaviors, Mental and Physical Health among Older Adults under Severe Lockdown Restrictions during the COVID-19 Pandemic in Spain. Int J Environ Res Public Health. 2021 July 01;18(13):7067. DOI: 10.3390/ijerph18137067
9. Delussi M, Gentile E, Coppola G, Prudenzano AMP, Rainero I, Sances G, Abagnale C, Caponnetto V, De Cesaris F, Frattale I, Guaschino E, Marcinnò A, Ornello R, Pistoia F, Putortì A, Roca ME, Roveta F, Lupi C, Trojano M, Pierelli F, Geppetti P, Sacco S, de Tommaso M. Investigating the Effects of COVID-19 Quarantine in Migraine: An Observational Cross-Sectional Study From the Italian National Headache Registry (RICe). Front Neurol. 2020 Nov 10;11:597881. DOI: 10.3389/fneur.2020.597881
10. Meng Q, Li N, Han X, Shao F, Wang W. Peri-adolescence isolation rearing alters social behavior and nociception in rats. Neurosci Lett. 2010; 480(1):25-29. DOI: 10.1016/j.neulet.2010.05.067
11. Graf AP, Hansson AC, Spanagel R. Isolated during adolescence: long-term impact on social behavior, pain sensitivity, and the oxytocin system in male and female rats. Biol Sex Differ. 2024 Oct 15;15(1):78. DOI: 10.1186/s13293-024-00655-7
12. Tuboly G, Benedek G, Horvath G. Selective disturbance of pain sensitivity after social isolation. Physiol Behav. 2009;96(1):18-22. DOI: 10.1016/j.physbeh.2008.07.030
13. Yazdanfar N, Ali Mard S, Mahmoudi J, Bakhtiari N, Sarkaki A, Farnam A. Maternal Morphine Exposure and Post-Weaning Social Isolation Impair Memory and Ventral Striatum Dopamine System in Male Offspring: Is an Enriched Environment Beneficial? Neuroscience. 2021 May 01;461:80-90. Epub 2021 Mar 02. DOI: 10.1016/j.neuroscience.2021.02.024
14. Ширенова С.Д., Крупина Н.А., Хлебникова Н.Н. Динамика болевой чувствительности у самцов и самок крыс в условиях длительной социальной изоляции. Российский журнал боли, 2019;17(4):27-34. DOI: 10.25731/RASP.2019.04.38
Shirenova SD, Krupina NA, Khlebnikova NN. Dynamics of pain sensitivity in male and female rats under prolonged social isolation. Russian Journal of Pain. 2019;17(4):27-34. (In Russ.). DOI: 10.25731/RASP.2019.04.38
15. Shirenova SD, Khlebnikova NN, Narkevich VB, Kudrin VS, Krupina NA. Nine-month-long Social Isolation Changes the Levels of Monoamines in the Brain Structures of Rats: A Comparative Study of Neurochemistry and Behavior. Neurochem Res. 2023 June; 48(6):1755-1774. Epub 2023 Jan 21. DOI: 10.1007/s11064-023-03858-3
16. Крупина Н.А., Хлебникова Н.Н. Длительная социальная изоляция ухудшает обучение в задаче двустороннего активного избегания у самок крыс. Журнал высшей нервной деятельности им. И.П. Павлова. 2024; 74(6):727-741. DOI: 10.1007/s11055-025-01810-2
10.31857/S0044467724060076. DOI: 10.1007/s11055-025-01810-2
17. McEwen BS, Gianaros PJ. Stress- and allostasis-induced brain plasticity. Annu Rev Med. 2011;62:431-445. DOI: 10.1146/annurev-med-052209-100430
18. Goel N, Workman JL, Lee TT, Innala L, Viau V. Sex differences in the HPA axis. Compr Physiol. 2014;4(3):1121-1125. DOI: 10.1002/cphy.c130054
19. Hodes GE, Bangasser D, Sotiropoulos I, Kokras N, Dalla C. Sex Differences in Stress Response: Classical Mechanisms and Beyond. Curr Neuropharmacol. 2024;22(3):475-494. DOI: 10.2174/1570159X22666231005090134
20. Ширенова С.Д., Хлебникова Н.Н., Крупина Н.А. Экспрессия рецепторов глюкокортикоидов и интерлейкинов IL-1β и IL-6 в структурах мозга крыс, подвергнутых длительной социальной изоляции: половые различия. Патогенез. 2022;20(3):147-148. DOI: 10.25557/2310-0435.2022.03.147-148
Shirenova SD, Khlebnikova NN, Krupina NA. Expression of receptors for glucocorticoids and interleukins IL-1β and IL-6 in brain structures of rats subjected to long-term social isolation: gender differences. Patogenez=Pathogenesis. 2022;20(3):147-148. (In Russ.). DOI: 10.25557/2310-0435.2022.03.147-148
21. Pape K, Tamouza R, Leboyer M, Zipp F. Immunoneuropsychiatry - novel perspectives on brain disorders. Nat Rev Neurol. 2019 June;15(6):317-328. DOI: 10.1038/s41582-019-0174-4
22. Barnes PJ. Glucocorticosteroids. Handb Exp Pharmacol. 2017;237:93-115. DOI: 10.1007/164_2016_62
23. Finnell JE, Muniz BL, Padi AR, Lombard CM, Moffitt CM, Wood CS, Wilson LB, Reagan LP, Wilson MA, Wood SK. Essential role of ovarian hormones in susceptibility to the consequences of witnessing social defeat in female rats. Biol Psychiatry. 2018;84(5):372-382.
24. Lovick TA, Zangrossi H Jr. Effect of Estrous Cycle on Behavior of Females in Rodent Tests of Anxiety. Front Psychiatry. 2021 Aug 31;12:711065. PMID: 34531768; PMCID: PMC8438218. DOI: 10.3389/fpsyt.2021.711065 EDN: XGLGHX PMID: 34531768
25. Yang C-X, Wang Y, Lu Q, Lian Y-N, Anto EO, Zhang Y, Wang W. Chronic stress influences nociceptive sensitivity of female rats in an estrous cycle-dependent manner. Stress. 2020 July;23(4):386-392. Epub 2019 Nov 14. DOI: 10.1080/10253890.2019.1687683
26. Shirenova SD, Khlebnikova NN, Krupina NA. Heat nociception in socially isolated female rats: The estrus cycle effects. International Webinar on Neurology & Therapeutics (IWNT). “Emerging Challenges and Advances in Neurology & Therapeutics”, London, March 08-09, 2021. Frontiers Meetings Ltd. 2021:22.
27. Wiesenfeld-Hallin Z. Sex differences in pain perception. Gend Med. 2005 Sept;2(3):137-145. DOI: 10.1016/s1550-8579(05)80042-7
28. Mogil JS, Chesler EJ, Wilson SG, Juraska JM, Sternberg WF. Sex differences in thermal nociception and morphine antinociception in rodents depend on genotype. Neurosci Biobehav Rev. 2000 May;24(3):375-389. DOI: 10.1016/s0149-7634(00)00015-4
29. Lima M, Malheiros J, Negrigo A, Tescarollo F, Medeiros M, Suchecki D, Tannús A, Guinsburg R, Covolan L. Sex-related long-term behavioral and hippocampal cellular alterations after nociceptive stimulation throughout postnatal development in rats. Neuropharmacology. 2014 Feb;77:268-276. Epub 2013 Oct 19. DOI: 10.1016/j.neuropharm.2013.10.007
30. Vierck CJ, Acosta-Rua AJ, Rossi HL, Neubert JK. Sex differences in thermal pain sensitivity and sympathetic reactivity for two strains of rat. J Pain. 2008 Aug;9(8):739-749. Epub 2008 May 16. DOI: 10.1016/j.jpain.2008.03.008
31. Bourgeois JR, Feustel PJ, Kopec AM. Sex differences in choice-based thermal nociceptive tests in adult rats. Behav Brain Res. 2022 July 05;429:113919. Epub 2022 May 04. DOI: 10.1016/j.bbr.2022.113919
32. Timmers I, Kaas AL, Quaedflieg CWEM, Biggs EE, Smeets T, de Jong JR. Fear of pain and cortisol reactivity predict the strength of stress-induced hypoalgesia. Eur J Pain. 2018 Aug;22(7):1291-1303. Epub 2018 Apr 19. DOI: 10.1002/ejp.1217
33. Butler RK, Finn DP. Stress-induced analgesia. Prog Neurobiol. 2009 July; 88(3):184-202. Epub 2009 Apr 22. DOI: 10.1016/j.pneurobio.2009.04.003
34. Vendruscolo LF, Pamplona FA, Takahashi RN. Strain and sex differences in the expression of nociceptive behavior and stress-induced analgesia in rats. Brain Res. 2004 Dec 31;1030(2):277-283. DOI: 10.1016/j.brainres.2004.10.016
35. Geva N, Defrin R. Opposite Effects of Stress on Pain Modulation Depend on the Magnitude of Individual Stress Response. J Pain. 2018 Apr;19(4): 360-371. Epub 2017 Dec 11. DOI: 10.1016/j.jpain.2017.11.011
36. Gera O, Ginzburg K, Gur N, Defrin R. Effects of acute stress exposure on pain sensitivity: the role of individual stress responsiveness and orientation to pain and stress. Pain. 2025 Oct 1;166(10):e388-e396. 10.1097/j.pain.0000000 2025 May 9. PMID: 40359374.000003622. Epub. DOI: 10.1097/j.pain.00000002025May9..000003622
37. Lian Y-N, Chang J-L, Lu Q, Wang Y, Zhang Y, Zhang F-M. Effects of fluoxetine on changes of pain sensitivity in chronic stress model rats. Neurosci Lett. 2017 June 09;651:16-20. Epub 2017 Apr 29. DOI: 10.1016/j.neulet.2017.04.062
38. Schneider SK, Pauli P, Lautenbacher S, Reicherts P. Effects of psychosocial stress and performance feedback on pain processing and its correlation with subjective and neuroendocrine parameters. Scand J Pain. 2022 Aug 09; 23(2):389-401. DOI: 10.1515/sjpain-2021-0204
39. Krupina NA, Shirenova SD, Khlebnikova NN. Prolonged Social Isolation, Started Early in Life, Impairs Cognitive Abilities in Rats Depending on Sex. Brain Sci. 2020 Oct 30;10(11):799. DOI: 10.3390/brainsci10110799
40. Raut A, Ratka A. Oxidative damage and sensitivity to nociceptive stimulus and opioids in aging rats. Neurobiol Aging. 2009 June;30(6):910-919. Epub 2007 Nov 07. DOI: 10.1016/j.neurobiolaging.2007.09.010
41. Tinnirello A, Mazzoleni S, Santi C. Chronic Pain in the Elderly: Mechanisms and Distinctive Features. Biomolecules. 2021 Aug 23;11(8):1256. DOI: 10.3390/biom11081256
42. Monroe TB, Gore JC, Bruehl SP, Benningfield MM, Dietrich MS, Chen LM, Newhouse P, Fillingim R, Chodkowski B, Atalla S, Arrieta J, Damon SM, Blackford JU, Cowan RL. Sex differences in psychophysical and neurophysiological responses to pain in older adults: a cross-sectional study. Biol Sex Differ. 2015 Nov 16;6:25.
Выпуск
Другие статьи выпуска
Цель исследования. Провести анализ публикаций, посвященных истории развития взглядов на проблему фантомно-болевого синдрома, изучению патогенетических механизмов и лечению данного болевого синдрома.
Материал и методы. Поиск публикаций проведен по базам данных eLibrary, PubMed, Google Scholar, CyberLeninka, Cochrane Library и по электронному каталогу ФГБУ «Российсая государственная библиотека». В анализ включались источники разных лет, имеющие значимые результаты для понимания проблемы фантомно-болевого синдрома, а также источники, имеющие историческую ценность для понимания этапов развития взглядов на проблему.
Результаты. Первое упоминание фантомно-болевого синдрома датируется XVI веком, но до настоящего времени продолжают уточняться патофизиологические механизмы, лежащие в основе развития данного болевого синдрома. Во многом сложности в подборе эффективного лечения обусловлены вовлечением в патогенез фантомной боли многочисленных структур периферической и центральной нервной системы. Анализ исследований показал, что предложенные разнообразные методики лечения не всегда способны избавить пациента от фантомной боли.
Заключение. Современные патофизиологические концепции возникновения и хронизации фантомно-болевого синдрома указывают на необходимость использования для достижения эффективного лечения у одного пациента как медикаментозных, так и немедикаментозных средств.
Дегенеративные поражения позвоночника могут проявляться скелетно-мышечной болью и радикулопатией. Ежегодно в мире регистрируется около 266 млн новых случаев симптомных дегенеративных заболеваний поясничного отдела позвоночника. В основе патологии лежит дегенерация межпозвонкового диска, одним из ключевых факторов развития которой являются провоспалительные цитокины, а также активация металлопротеиназ и механотрансдукция через каналы Piezo1. В обзоре проанализированы патогенетические механизмы дегенеративных поражений позвоночника и проведена оценка эффективности и безопасности системных глюкокортикостероидов при боли в спине дегенеративного генеза на основе клинических исследований последних лет. Показано, что, несмотря на способность глюкокортикостероидов подавлять ключевые медиаторы воспаления, их клиническая эффективность ограниченна: при радикулопатии отмечается лишь кратковременное улучшение, при скелетно-мышечной боли — отсутствие преимуществ перед терапией нестероидными противовоспалительными средствами, при стенозе — отсутствие эффекта. При этом существует риск развития тяжелых осложнений у людей из группы риска (гипертоническая болезнь, сахарный диабет) даже при коротких курсах лечения. Системное применение глюкокортикостероидов для лечения болей в спине при дегенеративных поражениях позвоночника не рекомендовано из-за низкого профиля по соотношению польза/риск.
Лечение пациентов с головной болью напряжения (ГБН) на сегодняшний день направлено на купирование эпизодов головной боли анальгетиками и на уменьшение количества дней с головной болью антидепрессантами. Перспективным направлением является использование миорелаксантов у пациентов с ГБН с мышечным напряжением.
Цель исследования. Изучение эффективности и безопасности эперизона (Стезиум) для лечения пациентов с головной болью напряжения в условиях реальной клинической практики.
Материал и методы. В исследование вошло 30 пациентов (18 мужчин и 12 женщин, средний возраст 39,8±13,9 года). Диагноз частой эпизодической ГБН был у 6 (20%) пациентов, хронической ГБН — у 24 (80%) пациентов.
Результаты. На фоне 8-недельного курса лечения эперизоном (Стезиум, таблетки с пролонгированным высвобождением, покрытые пленочной оболочкой, АО «Валента Фарм», Россия, в дозе 75 мг перорально 2 раза в сутки) у пациентов с ГБН происходило статистически значимое снижение количества дней с болью. Так, до лечения в группе в среднем отмечалось 25,0±7,7 дня с ГБН, а после лечения — 11,7±11,6 дня (p<0,001). Интенсивность боли снизилась с 3,8±1,1 балла до 2,5±1,5 балла по визуально-аналоговой шкале (p<0,001). Уровень мышечного напряжения статистически значимо уменьшился в перикраниальных мышцах. Доля пациентов-респондеров на терапию эперизоном составила 63,3% (n=19).
Заключение. Оценка напряжения височных и жевательных мышц в рамках пальпаторной альгометрии может быть использована как предиктор эффективности эперизона у пациентов с головной болью напряжения. Эперизон (Стезиум) может быть рекомендован для комплексного лечения пациентов с головной болью напряжения с мышечным напряжением.
Синдром взрывающейся головы (СВГ) — редкий синдром, ассоциированный со сном, характеризующийся повторяющимися кратковременными приступами ощущения внезапного громкого звука в голове, от которых пациент пробуждается. Согласно Международной классификации нарушений сна 3-го пересмотра (2014), СВГ относится к парасомниям. В литературе отмечена коморбидность СВГ и мигрени. Приводим описание клинического случая СВГ у пациентки с мигренью без ауры и краткий обзор литературы на эту тему.
Цель исследования. 1. Дополнить раздел «Вождение» Индекса ограничения жизнедеятельности из-за боли в шее (далее — Индекс) информацией, оценивающей влияние боли в шее на способность совершать поездки с использованием как общественного, так и личного транспорта. 2. Оценить психометрические свойства модифицированной версии опросника.
Материал и методы. Объект исследования — модифицированная (2020) русскоязычная версия Индекса. На первом этапе провели ретроспективный анализ заполненных анкет и рассчитали процент пропусков для раздела «Вождение». На втором этапе модифицировали раздел «Вождение» и оценили психометрические свойства новой версии опросника. Участники исследования — 337 пациентов (221 женщина и 116 мужчин) в возрасте от 18 до 65 лет (средний возраст 39,6±10,4 года) с неспецифической болью в шее (БШ), головной болью напряжения, мигренью и цервикогенной головной болью (ЦГБ).
Результаты. Ретроспективный анализ показал, что раздел «Вождение» был пропущен в 83 (43%) из 194 анкет, заполненных пациентами с БШ. Для устранения пропусков название этого раздела изменили на «Поездки на транспорте / вождение», а каждое утверждение дополнили фразой «Я езжу на транспорте…», например: «Я езжу на транспорте / вожу машину вообще без боли в шее». Эта модификация исключила пропуски при заполнении анкет. Опросник показал хорошую внутреннюю согласованность: α Кронбаха=0,89, коэффициент межпунктовой корреляции=0,47. Факторный анализ выявил двухфакторную структуру Индекса; во 2-м факторе максимальными факторными нагрузками обладали разделы «Головная боль» (0,878) и «Концентрация внимания» (0,876). Кластерный анализ выявил три отдельных непересекающихся кластера пациентов без ограничения жизнедеятельности, с легким и с умеренным ограничением жизнедеятельности. Группа без ограничения жизнедеятельности состояла преимущественно из пациентов с неспецифической БШ. Группа с умеренным ограничением жизнедеятельности состояла преимущественно из пациентов с хронической мигренью, в том числе сочетавшейся с хронической ЦГБ.
Заключение. Индекс ограничения жизнедеятельности из-за боли в шее, модифицированный для оценки способности пациентов совершать поездки на транспорте, — надежный инструмент, обладающим хорошими психометрическими свойствами, готовый к использованию как в повседневной практике, так и в клинических исследованиях.
Цель исследования. Изучить изменения болевой чувствительности у самок крыс при экспериментальном артрите височнонижнечелюстного сустава в условиях иммуномодуляции.
Материал и методы. Исследование проведено на половозрелых самках крыс (n=51). Сформированы пять экспериментальных групп: 1-я группа — интактные животные; 2-я группа — введение препарата «Имунофан» на 2-е, 4-е, 6-е, 8-е и 10-е сутки исследования; 3-я группа — инъекция монойодацетата натрия (МИА) в височно-нижнечелюстной сустав (ВНЧС) в 1-е сутки исследования; 4-я группа — инъекция МИА в ВНЧС в 1-е сутки исследования с последующим введением «Имунофана» на 2-е, 4-е, 6-е, 8-е и 10-е сутки исследования; 5-я группа — инъекция МИА в ВНЧС в 1-е сутки исследования с последующим введением «Имунофана» на 14-е, 16-е, 18-е, 20-е и 22-е сутки исследования. Порог болевой реакции животных изучали по латентному периоду реакции отведения хвоста при светотермальном раздражении методом tail-flick. Измерения выполняли в фазу диэструса эстрального цикла, определяемую путем микроскопии вагинальных мазков.
Результаты. Снижение латентного периода реакции отведения хвоста, характерное для животных, получивших инъекцию монойодацетата натрия в ВНЧС, не происходит в условиях иммуномодуляции. Указанный эффект «Имунофана» не зависит от времени начала применения препарата.
Заключение. Введение иммуномодулирующего препарата «Имунофан» самкам крыс в относительно ранние сроки формирования артрита височно-нижнечелюстного сустава, вызванного внутрисуставной инъекцией монойодацетата натрия, предупреждает усиление ноцицептивной чувствительности. Применение данного препарата на позднем этапе развития исследуемой патологии приводит к увеличению порога болевой реакции у животных с экспериментальным артритом височно-нижнечелюстного сустава.
Цель исследования. Изучение влияния пептидов GHK, PGP и GHK-PGP на спинальные и супраспинальные механизмы формирования температурной болевой чувствительности у крыс.
Материал и методы. Эксперименты выполнены на 100 крысах-самцах Wistar массой 170—190 г. В работе были использованы пептиды, синтезированные в Национальном исследовательском центре «Курчатовский институт»: GHK (Gly-His-Lys), PGP (Pro-Gly-Pro), GHK-PGP (Gly-His-Lys-Pro-Gly-Pro). Пептиды вводили внутрибрюшинно в дозах 0,5 мкг/кг, 5,0 мкг/кг и 50,0 мкг/кг однократно за 15 мин до начала эксперимента. Контрольным животным вводили эквивалентные объемы физиологического раствора. Болевую чувствительность изучали с использованием теста горячей пластины (hot-plate) и теста отдергивания хвоста от теплового излучения (tail-flick).
Результаты. Установлено, что пептид GHK обладает анальгетическим эффектом при боли, вызванной температурным раздражением в тесте горячей пластины, в дозах 0,5 мкг/кг и 50,0 мкг/кг. У пептида PGP обнаружено анальгетическое действие в минимальной исследуемой дозе. При этом пептид GHK-PGP обладает выраженным анальгетическим действием во всех исследуемых дозах, согласно результатам исследования, в тесте горячей пластины, а также в дозе 0,5 мкг/кг в тесте отдергивания хвоста от теплового излучения.
Заключение. Пептиды GHK и PGP обладают анальгетическим эффектом. При этом присоединение PGP к С-концу аминокислотной последовательности GHK потенцирует анальгетическое действие, которое проявляется во всех исследованных дозах. Также пептид GHK-PGP демонстрирует анальгетическое действие в тесте отдергивания хвоста от теплового излучения, что свидетельствует об активации сегментарных механизмов болевой чувствительности.
Введение. Фибромиалгия (ФМ) — хроническое болевое состояние, характеризующееся генерализованной болью, сопровождающейся утомляемостью, нарушением сна и когнитивных функций. От 0,2% до 6% населения мира страдает фибромиалгией. ФМ относится к дисфункциональным болевым синдромам, развитие которых обусловлено не повреждением тканей, а нарушением механизмов регуляции в системе болевой чувствительности. Патогенез ФМ сложен и обусловлен целым рядом факторов. В связи с этим разработка экспериментальной модели ФМ для изучения механизмов развития данного заболевания представляется актуальной.
Цель исследования. Разработать экспериментальную модель генерализованной боли у крыс посредством интермиттирующего стрессорного воздействия.
Материал и методы. Опыты проведены на трех группах животных: 1-я группа — интактный контроль; 2-я группа — животные, подвергнутые воздействию изоляции; 3-я группа — животные, подвергнутые сочетанному воздействию изоляционного и повторяющегося холодового стресса (ИПХС). Оценку изменения порогов болевой реакции (ПБР) у животных проводили с помощью электронного алгезиметра Рэндалла—Селитто (IITC, США), а для измерения порога тактильной чувствительности (ПТЧ) использовали эстезиометр фон Фрея с набором филаментов SupertipsTM (IITC, США) диаметром 0,8 мм с силой воздействия от 0,4 до 74 г. Измерения проводили за сутки до начала эксперимента, а также в 1-й, на 7-й, 14-й и 21-й день после его окончания.
Результаты. Разработана экспериментальная модель генерализованной боли с использованием перемежающегося пролонгированного психологического и холодового стрессорного воздействия.
Заключение. Результаты проведенного исследования свидетельствуют об обоснованности использования модели интермиттирующего стрессорного воздействия в качестве экспериментальной модели генерализованной боли.
Цель исследования. Изучить в эксперименте антиноцицептивную активность агониста каннабиноидного СВ1-рецептора производного 2H-хромена (шифр — CHR) на моделях послеоперационной и нейропатической боли, оценить вклад потенциального антиэкссудативного эффекта в механизм его антиноцицептивного действия.
Материал и методы. Исследование выполняли на мышах CD-1 и крысах Sprague Dawley. Животным в желудок вводили производное 2H-хромена CHR в эффективной дозе 5 мг/кг. Антиноцицептивную активность соединения CHR оценивали на моделях послеоперационной и нейропатической боли в сравнении с действием трамадола в дозе 20 мг/кг и габапентина в дозе 100 мг/кг. Антиэкссудативное и антиноцицептивное влияние соединения CHR исследовали при однократном введении крысам на модели отека задней конечности, вызванного каррагенином, сравнивали с эффектами диклофенака натрия в дозе 10 мг/кг.
Результаты. Соединение CHR повышало болевой порог на модели послеоперационной боли в 40 раз, при экспериментальной нейропатической боли — с 1-го по 7-й день исследования в 3,5 раза, 70 раз и 100 раз соответственно. Антиноцицептивный эффект соединения CHR выражен не слабее действия трамадола и габапентина. На модели отека задней конечности вещество CHR ослабляло экссудацию на 42%, диклофенак натрия уменьшал экссудацию на 67%, оба соединения увеличивали болевой порог в 15 раз (p<0,05).
Заключение. Производное 2H-хромена CHR в эффективной дозе 5 мг/кг оказывает выраженное антиноцицептивное действие при экспериментальной послеоперационной и нейропатической боли. Соединение CHR препятствует развитию экссудации слабее диклофенака натрия, но в такой же степени оказывает антиноцицептивное действие.
Статистика статьи
Статистика просмотров за 2026 год.
Издательство
- Издательство
- МЕДИА СФЕРА
- Регион
- Россия, Москва
- Почтовый адрес
- Издательство «Медиа Сфера», а/я 54, Москва, Россия, 127238
- Юр. адрес
- 127238, город Москва, Дмитровское ш, д. 46 к. 2 стр. 2
- ФИО
- Немцова Нина Валерьевна (ГЕНЕРАЛЬНЫЙ ДИРЕКТОР)
- E-mail адрес
- info@mediasphera.ru
- Контактный телефон
- +7 (495) 4824329