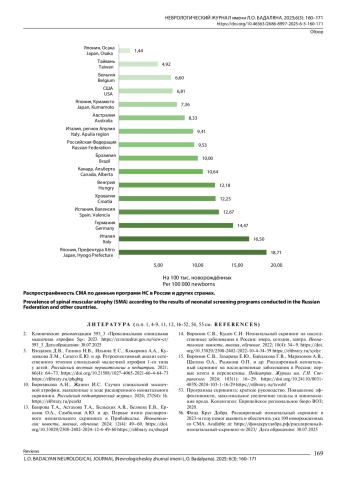
Цель статьи — представить актуальный статус и результаты программ неонатального скрининга (НС) на спинальную мышечную атро- фию (СМА), а также выполнить сравнительный анализ подходов к проведению НС, реализуемых в России и ряде зарубежных стран. СМА — одно из наиболее распространённых наследственных нервно-мышечных заболеваний, приводящее к ранней гибели пациен- тов детского возраста. В мировой практике наблюдается тенденция к расширению национальных программ НС и включению в них диагностики СМА. Ключевыми этапами в выявлении СМА являются первичное определение пациентов высокого риска методом коли- чественной ПЦР и дальнейшая подтверждающая диагностика, наиболее часто проводимая методом MLPA. По результатам анализа пи- лотных проектов НС на СМА в мире, наибольшая распространённость заболевания достигала 18,71 случая на 100 тыс. новорождённых и была выявлена в Японии (префектура Хёго). В европейских странах наибольшая распространённость СМА определялась в Италии, Германии, Испании (Валенсия). В России, согласно результатам расширенного НС, распространённость СМА составила 9,5 на 100 тыс. обследованных новорождённых. Появление эффективной терапии патогенетического действия предопределяет целесообразность выявления заболевания на его пресимптоматической стадии для достижения лучших результатов по клинически значимым исходам в долгосрочной перспективе. В настоящий момент на территории России зарегистрировано 3 лекарственных препарата патогенетиче- ского действия: нусинерсен, рисдиплам и онасемноген абепарвовек, что подтверждает значимость включения СМА в программу НС.
Идентификаторы и классификаторы
Спинальная мышечная атрофия (СМА) является наследственным нервно-мышечным заболеванием, характеризующимся прогрессирующей дегенерацией α-мотонейронов спинного мозга, развитием вялого паралича и мышечной атрофии [1, 2]. Клиническая картина СМА может варьировать в зависимости от возраста, в котором наблюдалась манифестация заболевания, и характеризоваться как быстропрогрессирующим течением и гибелью пациента или развитием необходимости в проведении респираторной поддержки в течение 1-го года жизни, так и более лёгким течением при проявлении заболевания во взрослом возрасте [3].
Если у вас возникли вопросы или появились предложения по содержанию статьи, пожалуйста, направляйте их в рамках данной темы.
Список литературы
1. Hjartarson H.T., Nathorst-Böös K., Sejersen T. Disease modifying therapies for the management of children with spinal muscular atrophy (5q SMA): an update on the emerging evidence. Drug Des. Devel. Ther. 2022; 16: 1865-83. DOI: 10.2147/dddt.s214174
2. Клинические рекомендации 593_3 “Проксимальная спинальная мышечная атрофия 5q”; 2023. https://cr.minzdrav.gov.ru/view-cr/593_3 Дата обращения: 30.07.2025.
3. Влодавец Д.В., Ганина Н.В., Ильина Е.С., Кокорина А.А., Кузенкова Л.М., Сапего Е.Ю. и др. Ретроспективный анализ естественного течения спинальной мышечной атрофии 1-го типа у детей. Российский вестник перинатологии и педиатрии. 2021; 66(4): 64-73. DOI: 10.21508/1027-4065-2021-66-4-64-73
4. Lee B.H., Deng S., Chiriboga C.A., Kay D.M., Irumudomon O., Laureta E., et al. Newborn Screening for Spinal Muscular Atrophy in New York State. Neurology. 2022; 99(14): e1527-37. DOI: 10.1212/wnl.0000000000200986
5. Aragon-Gawinska K., Mouraux C., Dangouloff T., Servais L. Spinal muscular atrophy treatment in patients identified by newborn screening - a systematic review. Genes (Basel). 2023; 14(7): 1377. DOI: 10.3390/genes14071377
6. Boardman F.K., Sadler C., Young P.J. Newborn genetic screening for spinal muscular atrophy in the UK: The views of the general population. Mol. Genet. Genomic Med. 2018; 6(1): 99-108. DOI: 10.1002/mgg3.353
7. Lee T., Tokunaga S., Taniguchi N., Fujino T., Saito M., Shimomura H., et al. Views of the general population on newborn screening for spinal muscular atrophy in Japan. Children (Basel). 2021; 8(8): 694. DOI: 10.3390/children8080694
8. Vrščaj E., Dangouloff T., Osredkar D., Servais L. Newborn screening programs for spinal muscular atrophy worldwide in 2023. J. Neuromuscul. Dis. 2024; 11(6): 1180-9. DOI: 10.1177/22143602241288095
9. SMA NBS Allians. About us. Available at: https://sma-screening-alliance.org/about-us Accessed July 30, 2025.
10. Боровикова А.Н., Жанин И.С. Случаи спинальной мышечной атрофии, выявленные в ходе расширенного неонатального скрининга. Российский педиатрический журнал. 2024; 27(S4): 16.
11. Mikhalchuk K., Shchagina O., Chukhrova A., Zabnenkova V., Chausova P., Ryadninskaya N., et al. Pilot program of newborn screening for 5q spinal muscular atrophy in the Russian Federation.Int. J. Neonatal Screen. 2023; 9(2): 29. DOI: 10.3390/ijns9020029
12. Kiselev A., Maretina M., Shtykalova S., Al-Hilal H., Maslyanyuk N., Plokhih M., et al. Establishment of a Pilot Newborn Screening Program for Spinal Muscular Atrophy in Saint-Petersburg.Int. J. Neonatal. Screen. 2024; 10(1): 9. DOI: 10.3390/ijns10010009
13. Баирова Т.А., Астахова Т.А., Бельских А.В., Беляева Е.В., Ершова О.А., Самбялова А.Ю. и др. Первые итоги расширенного неонатального скрининга в Прибайкалье. Неонатология: новости, мнения, обучение. 2024; 12(4): 49-60. DOI: 10.33029/2308-2402-2024-12-4-49-60
14. Воронин С.В., Куцев С.И. Неонатальный скрининг на наследственные заболевания в России: вчера, сегодня, завтра. Неонатология: новости, мнения, обучение. 2022; 10(4): 34-9. DOI: 10.33029/2308-2402-2022-10-4-34-39
15. Воронин С.В., Захарова Е.Ю., Байдакова Г.В., Марахонов А.В., Щагина О.А., Рыжкова О.П. и др. Расширенный неонатальный скрининг на наследственные заболевания в России: первые итоги и перспективы. Педиатрия. Журнал им. Г.Н. Сперанского. 2024; 103(1): 16-29. DOI: 10.24110/0031-403X-2024-103-1-16-29
16. SMA NBS Alliance. Status Map. Available at: https://sma-screening-alliance.org/map Accessed July 30, 2025.
17. Hegedűs K., Lénárt I., Xue A., Monostori P.B., Baráth Á., Mikos B., et al. Results of the Hungarian Newborn Screening Pilot Program for Spinal Muscular Atrophy.Int. J. Neonatal. Screen. 2025; 11(2): 29. DOI: 10.3390/ijns11020029
18. Boemer F., Caberg J.H., Beckers P., Dideberg V., di Fiore S., Bours V., et al. Three years pilot of spinal muscular atrophy newborn screening turned into official program in Southern Belgium. Sci. Rep. 2021; 11(1): 19922. DOI: 10.1038/s41598-021-99496-2
19. Berzal-Serrano A., García-Bohórquez B., Aller E., Jaijo T., Pitarch-Castellano I., Rausell D., et al. Outcomes of a pilot newborn screening program for spinal muscular atrophy in the Valencian community.Int. J. Neonatal. Screen. 2025; 11(1): 7. DOI: 10.3390/ijns11010007
20. Gagliardi D., Canzio E., Orsini P., Conti P., Sinisi V., Maggiore C., et al. Early spinal muscular atrophy treatment following newborn screening: A 20-month review of the first Italian regional experience. Ann. Clin. Transl. Neurol. 2024; 11(5): 1090-6. DOI: 10.1002/acn3.52018
21. Vill K., Kölbel H., Schwartz O., Blaschek A., Olgemöller B., Harms E., et al. One year of newborn screening for SMA - results of a German pilot project. In: Journal of Neuromuscular Diseases. London: SAGE Publications; 2019.
22. Vill K., Schwartz O., Blaschek A., Gläser D., Nennstiel U., Wirth B., et al. Newborn screening for spinal muscular atrophy in Germany: clinical results after 2 years. Orphanet J. Rare Dis. 2021; 16(1): 153. DOI: 10.1186/s13023-021-01783-8
23. Abiusi E., Vaisfeld A., Fiori S., Novelli A., Spartano S., Faggiano M.V., et al. Experience of a 2-year spinal muscular atrophy NBS pilot study in Italy: towards specific guidelines and standard operating procedures for the molecular diagnosis. J. Med. Genet. 2023; 60(7): 697-705. DOI: 10.1136/jmg-2022-108873
24. Cure SMA. Newborn Screening for SMA. Available at: https://curesma.org/newborn-screening-for-sma/Accessed July 30, 2025.
25. Hale K., Ojodu J., Singh S. Landscape of spinal muscular atrophy newborn screening in the United States: 2018-2021.Int. J. Neonatal Screen. 2021; 7(3): 33. DOI: 10.3390/ijns7030033
26. Zaidman C.M., Crockett C.D., Wedge E., Tabatabai G., Goedeker N. Newborn screening for spinal muscular atrophy: variations in practice and early management of infants with spinal muscular atrophy in the United States.Int. J. Neonatal Screen. 2024; 10(3): 58. DOI: 10.3390/ijns10030058
27. Wong K.N., McIntyre M., Cook S., Hart K., Wilson A., Moldt S., et al. A five-year review of newborn screening for spinal muscular atrophy in the State of Utah: lessons learned.Int. J. Neonatal Screen. 2024; 10(3): 54. DOI: 10.3390/ijns10030054
28. Baker M.W., Mochal S.T., Dawe S.J., Wiberley-Bradford A.E., Cogley M.F., Zeitler B.R., et al. Newborn screening for spinal muscular atrophy: The Wisconsin first year experience. Neuromuscul. Disord. 2022; 32(2): 135-41. DOI: 10.1016/j.nmd.2021.07.398
29. Elkins K., Wittenauer A., Hagar A.F., Logan R., Sekul E., Xiang Y., et al. Georgia state spinal muscular atrophy newborn screening experience: Screening assay performance and early clinical outcomes. Am. J. Med. Genet. C Semin. Med. Genet. 2022; 190(2): 187-96. DOI: 10.1002/ajmg.c.32003
30. Matteson J., Wu C.H., Mathur D., Tang H., Sciortino S., Feuchtbaum L., et al. California’s experience with SMA newborn screening: A successful path to early intervention. J. Neuromuscul. Dis. 2022; 9(6): 777-85. DOI: 10.3233/jnd-221561
31. Kraszewski J.N., Kay D.M., Stevens C.F., Koval C., Haser B., Ortiz V., et al. Pilot study of population-based newborn screening for spinal muscular atrophy in New York state. Genet. Med. 2018; 20(6): 608-13. DOI: 10.1038/gim.2017.152
32. Kay D.M., Stevens C.F., Parker A., Saavedra-Matiz C.A., Sack V., Chung W.K., et al. Implementation of population-based newborn screening reveals low incidence of spinal muscular atrophy. Genet. Med. 2020; 22(8): 1296-302. DOI: 10.1038/s41436-020-0824-3
33. Hale J.E., Darras B.T., Swoboda K.J., Estrella E., Chen J.Y.H., Abbott M.A., et al. Massachusetts’ findings from statewide newborn screening for spinal muscular atrophy.Int. J. Neonatal Screen. 2021; 7(2): 26. DOI: 10.3390/ijns7020026
34. Belter L., Taylor J.L., Jorgensen E., Glascock J., Whitmire S.M., Tingey J.J., et al. Newborn screening and birth prevalence for spinal muscular atrophy in the US. JAMA Pediatr. 2024; 178(9): 946-9. DOI: 10.1001/jamapediatrics.2024.1911
35. Groulx-Boivin E., Osman H., Chakraborty P., Lintern S., Oskoui M., Selby K., et al. Variability in newborn screening across Canada: spinal muscular atrophy and beyond. Can. J. Neurol. Sci. 2024; 51(2): 203-9. DOI: 10.1017/cjn.2023.34
36. McMillan H.J., Kernohan K.D., Yeh E., Amburgey K., Boyd J., Campbell C., et al. Newborn screening for spinal muscular atrophy: Ontario testing and follow-up recommendations. Can. J. Neurol. Sci. 2021; 48(4): 504-11. DOI: 10.1017/cjn.2020.229
37. Niri F., Nicholls J., Baptista Wyatt K., Walker C., Price T., Kelln R., et al. Alberta spinal muscular atrophy newborn screening - results from year 1 pilot project.Int. J. Neonatal Screen. 2023; 9(3): 42. DOI: 10.3390/ijns9030042
38. Kernohan K.D., McMillan H.J., Yeh E., Lacaria M., Kowalski M., Campbell C., et al. Ontario newborn screening for spinal muscular atrophy: the first year. Can. J. Neurol. Sci. 2022; 49(6): 821-3. DOI: 10.1017/cjn.2021.231
39. Romanelli Tavares V.L., Mendonça R.H., Toledo M.S., Hadachi S.M., Grindler C.M., Zanoteli E., et al.Integrated approaches and practical recommendations in patient care identified with 5q spinal muscular atrophy through newborn screening. Genes (Basel). 2024; 15(7): 858. DOI: 10.3390/genes15070858
40. Oliveira Netto A.B., Brusius-Facchin A.C., Lemos J.F., Pasetto F.B., Brasil C.S., Trapp F.B., et al. Neonatal screening for spinal muscular atrophy: A pilot study in Brazil. Genet. Mol. Biol. 2023; 46(3 Suppl. 1): e20230126. DOI: 10.1590/1678-4685-gmb-2023-0126
41. Chien Y.H., Chiang S.C., Weng W.C., Lee N.C., Lin C.J., Hsieh W.S., et al. Presymptomatic diagnosis of spinal muscular atrophy through newborn screening. J. Pediatr. 2017; 190: 124-9.e1. DOI: 10.1016/j.jpeds.2017.06.042
42. Weng W.C., Hsu Y.K., Chang F.M., Lin C.Y., Hwu W.L., Lee W.T., et al. CMAP changes upon symptom onset and during treatment in spinal muscular atrophy patients: lessons learned from newborn screening. Genet. Med. 2021; 23(2): 415-20. DOI: 10.1038/s41436-020-00987-w
43. Wang C.H., Hsu T.R., Liu M.Y., Wang L.Y., Chou I.J., Lee W.T., et al. Newborn screening facilitates early theranostics and improved spinal muscular atrophy outcome: five-year real-world evidence from Taiwan. Orphanet J. Rare Dis. 2025; 20(1): 197. DOI: 10.1186/s13023-025-03697-1
44. Sonehara S., Bo R., Nambu Y., Iketani K., Lee T., Shimomura H., et al. Newborn screening for spinal muscular atrophy: a 2.5-year experience in Hyogo prefecture, Japan. Genes (Basel). 2023; 14(12): 2211. DOI: 10.3390/genes14122211
45. Noguchi Y., Bo R., Nishio H., Matsumoto H., Matsui K., Yano Y., et al. PCR-based screening of spinal muscular atrophy for newborn infants in Hyogo prefecture, Japan. Genes (Basel). 2022; 13(11): 2110. DOI: 10.3390/genes13112110
46. Kimizu T., Nozaki M., Okada Y., Sawada A., Morisaki M., Fujita H., et al. Multiplex real-time PCR-based newborn screening for severe primary immunodeficiency and spinal muscular atrophy in Osaka, Japan: оur results after 3 years. Genes (Basel). 2024; 15(3): 314. DOI: 10.3390/genes15030314
47. Kimizu T., Ida S., Oki K., Shima M., Nishimoto S., Nakajima K., et al. Newborn screening for spinal muscular atrophy in Osaka-challenges in a Japanese pilot study. Brain Dev. 2023; 45(7): 363-71. DOI: 10.1016/j.braindev.2023.03.004
48. Sawada T., Kido J., Sugawara K., Yoshida S., Ozasa S., Nomura K., et al. Newborn screening for spinal muscular atrophy in Japan: оne year of experience. Mol. Genet. Metab. Rep. 2022; 32: 100908. DOI: 10.1016/j.ymgmr.2022.100908
49. D’Silva A.M., Kariyawasam D.S.T., Best S., Wiley V., Farrar M.A.Integrating newborn screening for spinal muscular atrophy into health care systems: an Australian pilot programme. Dev. Med. Child Neurol. 2022; 64(5): 625-32. DOI: 10.1111/dmcn.15117
50. Kariyawasam D.S.T., Russell J.S., Wiley V., Alexander I.E., Farrar M.A. The implementation of newborn screening for spinal muscular atrophy: the Australian experience. Genet. Med. 2020; 22(3): 557-65. DOI: 10.1038/s41436-019-0673-0
51. Efimova I.Y., Zinchenko R.A., Marakhonov A.V., Balinova N.V., Mikhalchuk K.A., Shchagina O.A., et al. Epidemiology of spinal muscular atrophy based on the results of a large-scale pilot project on 202,908 newborns. Pediatr. Neurol. 2024; 156: 147-54. DOI: 10.1016/j.pediatrneurol.2024.04.015
52. Šimić D., Šarić A., Škaričić A., Lehman I., Bunoza B., Rako I., et al. One-year pilot study results of newborn screening for spinal muscular atrophy in the Republic of Croatia.Int. J. Neonatal Screen. 2024; 10(3): 50. DOI: 10.3390/ijns10030050
53. Программы скрининга: краткое руководство. Повышение эффективности, максимальное увеличение пользы и минимизация вреда. Копенгаген: Европейское региональное бюро ВОЗ; 2020.
54. Cooper K., Nalbant G., Sutton A., Harnan S., Thokala P., Chilcott J., et al. Systematic review of presymptomatic treatment for spinal muscular atrophy.Int. J. Neonatal Screen. 2024; 10(3): 56. DOI: 10.3390/ijns10030056
55. Müller-Felber W., Blaschek A., Schwartz O., Gläser D., Nennstiel U., Brockow I., et al. Newbornscreening SMA - from pilot project to nationwide screening in Germany. J. Neuromuscul. Dis. 2023; 10(1): 55-65. DOI: 10.3233/jnd-221577
56. Фонд Круг Добра. Расширенный неонатальный скрининг в 2023-м году помог выявить и обеспечить уже 100 новорожденных со СМА. Available at: https://фондкругдобра.рф/расширенный-неонатальный-скрининг-в-2023/ Дата обращения: 30.07.2025.
Выпуск
Другие статьи выпуска
Боль является одним из самых распространённых немоторных симптомов болезни Паркинсона (БП), возникает у 85% пациентов на разных стадиях заболевания. Несмотря на высокую встречаемость, болевой синдром часто остаётся в «слепой зоне» диагноста и самого пациента, адаптированного к постоянному дискомфорту. Одной из причин недостаточного внимания к болевому синдрому при БП является отсутствие единого взгляда на классификацию и, как следствие, диагностического инструмента, который позволил бы систематически и объективно оценивать все аспекты болевого синдрома у пациентов с БП. В рамках настоящего обзора мы привели ведущие теории патогенеза болевого синдрома при БП, оценили их отражение в существующих классификациях, а также проанализировали практичность и эффективность шкал и опросников для оценки боли при БП. Особое внимание уделено ключевым подтипам боли, таким как ноцицептивная, нейропатическая и ноципластическая, и их значению в клинической практике. Принципиально новым аспектом, не освещённым в более ранних обзорах, является концепция Park-pain (болевого подтипа БП) — специфической формы течения БП, при которой боль становится ведущим немоторным симптомом, сопровождающимся выраженными психоэмоциональными нарушениями. Мы обнаружили, что текущие тенденции в понимании боли у пациентов с БП не отражены в действующих классификациях, что подчёркивает необходимость создания новой диагностической парадигмы, учитывающей современные представления о природе боли и влиянии её на качество жизни.
Цель статьи — анализ современных данных о роли уровня циркулирующих нейрофиламентов как биомаркёра спинальной мышечной атрофии (СМА) при генотерапии препаратом онасемноген абепарвовек. СМА — это орфанное наследственное аутосомно-рецессивное заболевание, обусловленное дефектами гена SMN1, кодирующего белок SMN. При СМА происходит гибель α-мотонейронов спинного мозга, приводящая к прогрессирующей мышечной слабости. Онасемноген абепарвовек — генозаместительная терапия, направленная на восстановление экспрессии белка SMN при СМА. В обзоре подчёркивается необходимость формирования панели биомаркёров для оценки тяжести СМА и эффективности терапии, поскольку клинические методы часто недостаточно чувствительны для мониторинга ответа на лечение. Нейрофиламенты — структурные белки аксонов, высвобождающиеся при повреждении нейронов, рассматриваются как перспективные биомаркеры, которые отражают степень нейродегенерации и динамику заболевания. На сегодняшний день количество исследований, посвящённых использованию циркулирующих нейрофиламентов при СМА при терапии препаратом онасемноген абепарвовек, невелико, что требует дальнейших клинических и лабораторных исследований для подтверждения их значимости. Обзор систематизирует данные о молекулярно-генетических основах патогенеза СМА, существующей на данный момент терапии и потенциале нейрофиламентов как биомаркёров при генотерапии препаратом онасемноген абепарвовек. Сделан вывод о необходимости дальнейших исследований в этой области для оптимизации персонализированного подхода к лечению пациентов со СМА.
Атаксический детский церебральный паралич (аДЦП) — наименее распространённая среди всех форм ДЦП, встречается реже, чем у 1 из 10 пациентов с ДЦП. К возрасту 5 лет более чем у половины из этих детей диагноз пересматривается, и подтверждаются другие состояния, не связанные с ДЦП. Накапливаются данные о том, что фенотипическое сходство с аДЦП может быть у ряда генетических заболеваний. Некоторые из них проявляются с рождения, другие манифестируют позже и имеют прогрессирующее течение.
Цель исследования — изучить особенности клинической картины, лабораторных и инструментальных данных, позволяющих отличить пациентов с аДЦП от пациентов с наследственными формами атаксий.
Материалы и методы. В исследование были включены 59 детей в возрасте от 1 года до 3 лет 8 мес, которые были распределены на 3 группы: с подтверждённым аДЦП (n = 29), наследственными заболеваниями (атаксия с подтверждённым генетическим диагнозом) (n = 13), прогрессирующей атаксией предположительно генетической природы, окончательно не верифицированной (n = 17). Всем детям проводились детальная оценка анамнеза, исследование неврологического статуса, нейровизуализация (МРТ). Выраженность двигательных нарушений оценивали с помощью шкалы GMFSC, а степень тяжести атаксии — по разработанной нами Педиатрической шкале атаксии (ПША). При исследовании с помощью ПША проводилась оценка в баллах развития моторных навыков и симптомов, указывающих на поражение структур ЦНС, отвечающих за координацию движений. По общей сумме баллов тяжесть атаксии рассматривали как лёгкую (1–8 баллов), среднюю (9–13 баллов) и тяжёлую (14–23 баллов). Все пациенты наблюдались в динамике на протяжении 5 лет.
Результаты. При включении в исследование между группами отсутствовали значимые различия средних балльных оценок по ПША, и у большинства пациентов определялась атаксия средней тяжести. Однако динамика оценок по ПША за 5-летний период наблюдения пациентов оказалась разнонаправленной: у детей с аДЦП они имели тенденцию к стабилизации и постепенному улучшению, тогда как для пациентов групп с наследственными и предположительно генетическими атаксиями характерным было их неуклонное ухудшение в связи с нарастанием двигательных расстройств. Следует подчеркнуть сходство динамики показателей по ПША у пациентов двух последних групп. По данным МРТ, в группе аДЦП преобладали изменения, типичные для гипоксически-ишемического поражения в виде перивентрикулярной лейкопатии (73,3%). Другой часто выявляемой патологией была гипоплазия мозжечка (46,4%). В группе наследственно обусловленной атаксии перивентрикулярная лейкопатия встречалась несколько реже (61,5%), другими находками были корковая атрофия (30,7%), гипомиелинизация (7,6%), гипоплазия ствола мозга (7,6%) и атрофия мозжечка (7,6%).
Заключение. Основными дифференциально-диагностическими критериями между наследственно обусловленными атаксиями и аДЦП являются прогрессирование клинической картины болезни, нарастание изменений на МРТ и молекулярно-генетическое выявление мутаций, которые вызывают заболевания, сопровождающиеся атаксией в детском возрасте.
Цель исследования — оценка динамики двигательной активности с помощью сбора анамнестических данных и динамического наблюдения за пациентами с миодистрофией Дюшенна, вызванной нонсенс-мутацией (нмМДД), в Московской области на фоне патогенетической терапии препаратом аталурен.
Материалы и методы. Динамическое наблюдение 13 пациентов с нмМДД осуществляли на базе Центра детской психоневрологии Научно-исследовательского клинического института детства Московской области. В данном исследовании проводился ретроспективный анализ анамнестических данных, двигательной активности пациентов по тестам «Северная Звезда» (NSAA) и 6-минутной ходьбы (6MWT). Для оценки эффективности терапии препаратом аталурен было проведено непрямое сравнение с данными из регистров STRIDE и CINRG DNHS.
Результаты. В исследуемой группе пациентов возраст начала самостоятельной ходьбы составил 15,7 ± 4,5 мес, возраст установки диагноза — 60,2 ± 21,7 мес (5,0 ± 1,8 года). 92% пациентов (n = 12) получают глюкокортикостероиды (ГКС), 5 из них — преднизолон, 7 — дефлазакорт. Средний возраст начала приёма ГКС составил 7,1 ± 0,9 года. Возраст инициации патогенетической терапии препаратом аталурен составил 7,0 ± 1,3 года. Длительность наблюдения пациентов варьировалась от 1,5 до 8 лет. Данные по пациентам с верифицированными результатами спирометрии (46%) и эхокардиографии (92%) за последние 12 мес распределились следующим образом: снижения фракции выброса левого желудочка не зарегистрировано ни у одного пациента, снижение форсированной жизненной ёмкости лёгких лёгкой степени наблюдалось у 1 пациента. Регулярные реабилитационные мероприятия получают 8 (62%) пациентов. Для оценки двигательных функций использовали тесты NSAA (n = 10) и 6MWT (n = 8). При анализе данных с помощью 6MWT наблюдалось увеличение пройденного расстояния у 6 (75%) пациентов, уменьшение — у 2 (25%). Результаты теста NSAA: у 2 (20%) пациентов отмечается улучшение, у 6 (60%) — стабилизация состояния, у 2 (20%) — ухудшение (в том числе у 1 — потеря амбулаторности).
Заключение. Своевременная диагностика и лечение пациентов в соответствии с клиническими рекомендациями играют ключевую роль в успешной терапии пациентов с МДД. Патогенетическая терапия препаратом аталурен замедляет скорость прогрессирования заболевания и улучшает выживаемость пациентов с нмМДД.
Возрастзависимые фокальные эпилепсии детства (ВЗФЭД) — наиболее часто встречающиеся эпилептические синдромы в детском возрасте, на их долю приходится около 15–20% форм заболевания в данной возрастной когорте. Особое внимание в проблеме ВЗФЭД уделяется эпилептиформной активности, имеющей тенденцию к усилению своей выраженности во время медленноволнового сна, чьё влияние на нейрокогнитивное развитие пациентов активно изучается. У части больных ВЗФЭД в течение активной стадии заболевания возможно формирование феномена продолженной спайк-волновой активации во сне, характерного для одноимённых синдромов эпилептических энцефалопатий.
Цель исследования: оценить влияние эпилептиформной активности на состояние интеллектуальных функций у детей с синдромами ВЗФЭД.
Материалы и методы. В исследование были включены 34 ребёнка с диагностированным синдромом ВЗФЭД; диагноз установлен на основании данных анамнеза, неврологического и инструментального обследований. Всем детям проведено видео-ЭЭГ-мониторирование сна с целью подсчёта спайк-волнового индекса (СВИ), исследование с использованием теста интеллекта Векслера (детский вариант) и шкалы адаптивного поведения Вайнленд-2.
Результаты. Увеличение СВИ более чем на 50% отмечено у 13 (38,2%) пациентов, причём у 8 (23,2%) пациентов регистрировался феномен продолженной спайк-волновой активации во сне. При исследовании уровня интеллекта по методу Векслера получены следующие средние значения: вербальный IQ — 103,15, невербальный IQ — 111,03, общий IQ — 107,12. Выявлены обратные корреляционные связи между значением СВИ и показателями интеллектуального развития, СВИ и показателями адаптивного поведения.
Заключение. Высокий уровень СВИ оказывает значительное влияние на показатели интеллектуального развития у детей с синдромами ВЗФЭД. Обратная корреляция между значениями СВИ и показателями IQ указывает на важность контроля индекса эпилептиформной активности для предотвращения когнитивных нарушений, что особенно важно не только для детей с синдромами эпилептических энцефалопатий со спайк-волновой активацией во сне, но и для пациентов с ВЗФЭД. Установлено достоверное снижение показателей IQ с возрастом у детей с синдромами ВЗФЭД, что требует дальнейшего изучения.
Статистика статьи
Статистика просмотров за 2026 год.
Издательство
- Издательство
- НМИЦ здоровья детей
- Регион
- Россия, Москва
- Почтовый адрес
- 119991, город Москва, Ломоносовский пр-кт, д.2 стр.1
- Юр. адрес
- 119991, город Москва, Ломоносовский пр-кт, д.2 стр.1
- ФИО
- Фисенко Андрей Петрович (ДИРЕКТОР)
- E-mail адрес
- director@nczd.ru
- Контактный телефон
- +7 (499) 1343083
- Сайт
- https://nczd.ru