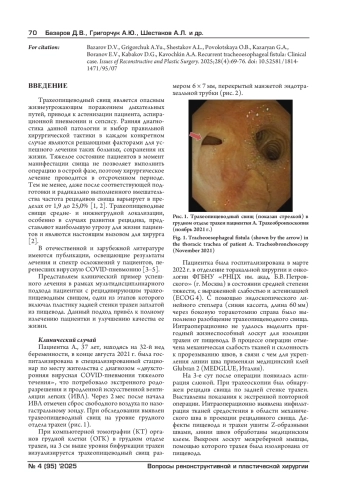
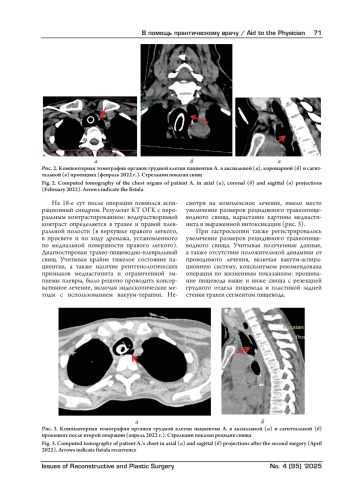
В статье описан нестандартный хирургический подход к лечению пациентки с рецидивирующим трахеопищеводным свищом. Применен метод пластики задней стенки трахеи заплатой из пищевода. Такой подход в условиях дефицита тканей и длительно существующей инфекции позволил изолировать пораженный участок задней стенки трахеи и создать дополнительную защиту механического шва. Выбранный подход привел к полному излечению и улучшению качества жизни пациентки.
Идентификаторы и классификаторы
Трахеопищеводный свищ является опасным жизнеугрожающим поражением дыхательных путей, приводя к астенизации пациента, аспирационной пневмонии и сепсису. Ранняя диагностика данной патологии и выбор правильной хирургической тактики в каждом конкретном случае являются решающими факторами для успешного лечения таких больных, сохранения их жизни. Тяжелое состояние пациентов в момент манифестации свища не позволяет выполнить операцию в острой фазе, поэтому хирургическое лечение проводится в отсроченном периоде. Тем не менее, даже после соответствующей подготовки и радикально выполненного вмешательства частота рецидивов свища варьирует в пределах от 1,9 до 25,0% [1, 2]. Трахеопищеводные свищи средне- и нижнегрудной локализации, особенно в случаях развития рецидива, представляют наибольшую угрозу для жизни пациентов и являются настоящим вызовом для хирурга [2].
Если у вас возникли вопросы или появились предложения по содержанию статьи, пожалуйста, направляйте их в рамках данной темы.
Список литературы
1. Aworanti O., Awadalla S. Management of Recurrent Tracheoesophageal Fistulas: A Systematic Review. Eur J Pediatr Surg. 2014; 24(05): 365-375. DOI: 10.1055/s-0034-1370780
2. Paraschiv M. Tracheoesophageal fistula - a complication of prolonged tracheal intubation. J Med Life. 2014;7(4):516-21.
3. Топольницкий Е.Б., Шефер Н.А., Капитанова Д.В., Подгорнов В.Ф. Лечение постреанимационных рубцовых стенозов трахеи после перенесенной коронавирусной пневмонии COVID-19. Хирургия. Журнал им. Н.И. Пирогова. 2022;4:5-10. DOI: 10.17116/hirurgia20220415
4. Brascia D., De Palma A., Cantatore M.G., Pizzuto O., Signore F., Sampietro D., Valentini M., Genualdo M., Marulli G. Not only acute respiratory failure: COVID-19 and the post-intubation/tracheostomy upper airways lesions. Front. Surg. 2023;10:1150254. DOI: 10.3389/fsurg.2023.1150254
5. Conforti S., Licchetta G., Reda M., Astaneh A., Pogliani L., Fieschi S., Rinaldo A., Torre M. Management of COVID-19-related post-intubation tracheal stenosis. Front. Surg. 2023; 10: 1129803. doi: 2.3389/fsurg.2023.1129803.
6. Паршин В.Д., Вишневская Г.А., Русаков М.А., Гудовский Л.М., Паршин В.В., Чернова Е.А. Трахеопищеводные свищи: современное состояние проблемы // Хирургия. Журнал им. Н.И. Пирогова. 2013. Т. 2. С. 73-79.
7. Muniappan A., Wain J.C., Wright C.D., Donahue D.M., Gaissert H., Lanuti M., Mathisen D.J. Surgical Treatment of Nonmalignant Tracheoesophageal Fistula: A Thirty-Five Year Experience. The Annals of Thoracic Surgery. 2013;95(4):1141-1146. DOI: 10.1016/j.athoracsur.2012.07.041
8. Ke M., Wu X., Zeng J. The treatment strategy for tracheoesophageal fistula. J Thorac Dis. 2015 Dec; 7(Suppl 4):S389-97. issn.2072-1439.2015.12.11. PMID: 26807286; PMCID: PMC4700364. DOI: 10.3978/j PMID: 26807286
9. Zhou C., Hu Y., Xiao Y., Yin W. Current treatment of tracheoesophageal fistula. Therapeutic Advances in Respiratory Disease. 2017;11(4):173-180. DOI: 10.1177/1753465816687518
10. Macchiarini P., Verhoye J.P., Chapelier A., Fadel E., Dartevelle P. Evaluation and outcome of different surgical techniques for postintubation tracheoesophageal fistulas. J Thorac Cardiovasc Surg. 2000;119(2):268-76. PMID: 10649202. DOI: 10.1016/S0022-5223(00)70182-6 PMID: 10649202
11. Топольницкий Е.Б., Дамбаев Г.Ц. Новая методика хирургического лечения трахеопищеводных свищей неопухолевого генеза // Бюллетень сибирской медицины. 2012. Т. 11, № 1. С. 91-96.
12. Bolca C., Pãvãloiu V., Fotache G., Dumitrescu M., Bobocea A., Alexe M., Cadar G., Stoica R., Paleru C., Cordos I. Postintubation Tracheoesophageal Fistula - Diagnosis, Treatment and Prognosis. Chirurgia. 2017;112(6):696- 704. DOI: 10.21614/chirurgia.112.6.696
13. Bolca C., Bobocea A., Cosoveanu G., Alexe M., Cadar G., Balescu I., Bacalbasa N., Gherghiceanu F., Furtunescu F., Radavoi D., Paleru C., Miron A., Cordos I. Acquired benign tracheo-oesophageal fistula secondary to oesophageal stenting for post lye ingestion stenosis: A case report. Experimental and Therapeutic Medicine. 2022;25(1):15. DOI: 10.3892/etm.2022.11714
14. Engel-Rodriguez A., Tiru-Vega M., Merced-Roman J., Fonseca-Ferrer V., Engel-Rodriguez N., Otero-Dominguez Y., Rodriguez-Cintron W. Diagnosis and Management of a Massive Eight-Centimeter Acquired Tracheoesophageal Fistula. Cureus. 2023;15(8):e43689. DOI: 10.7759/cureus.43689
15. Propst E.J., Ling S.C., Daneman A., Langer J.C. Endoscopic clip for closure of persistent tracheoesophageal fistula in an infant. Laryngoscope. 2014;124(9):2182. DOI: 10.1002/lary.24650
16. Jougon J., Couraud L. Esophageal patching for an unsuturable tracheoesophageal fistula. European Journal of Cardio-thoracic Surgery. 1998;14(4):431-433. DOI: 10.1016/S1010-7940(98)00226-7
17. Han Y., Liu K., Li X., Wang X., Zhou Y., Gu Z., Ma Q., Jiang T., Huang L, Zhang T., Cheng Q. Repair of massive stent-induced tracheoesophageal fistula. J Thorac Cardiovasc Surg. 2009 Apr;137(4):813-7. DOI: 10.1016/j.jtcvs.2008.07.050
18. Bardini R., Radicchi V., Parimbelli P., Tosato S.M., Narne S. Repair of a recurrent benign Tracheoesophageal fistula with a Gore-Tex membrane. The Annals of Thoracic Surgery. 2003;76(1):304-306. DOI: 10.1016/S0003-4975(02)04898-1
19. Wolf M., Segal E., Yellin A., Faibel M., Talmi Y.P., Kronenberg J. Acquired. Tracheoesophageal Fistula in Critically ill Patients. Annals of Otology, Rhinology & Laryngology. 2000;109(8):731-735. DOI: 10.1177/000348940010900806
20. Скворцов М.Б., Нечаев Е.В., Боричевский В.И. Трансорганное закрытие трахеопищеводного свища и последующее лечение его последствий // Сибирский медицинский журнал (Иркутск). 2015. Т. 133, № 2. С. 125-132.
Выпуск
Другие статьи выпуска
Цель исследования: оценить эффективность и подтвердить статус метода И. Понсети (I. Ponseti) как золотого стандарта консервативного лечения врожденной косолапости у детей раннего возраста на основе 10-летнего опыта работы отделения детской ортопедии ОГАУЗ «Больница скорой медицинской помощи № 2» (г. Томск).
Материал и методы. За последние 10 лет на базе отделения детской ортопедии ОГАУЗ БСМП № 2 (г. Томск) пролечено 168 детей в возрасте от 1 мес до 3 лет с врожденной косолапостью (198 стоп). Степень врожденной деформации до лечения оценивали в баллах по шкале A. Dimeglio, она варьировала от 15 до 20 баллов. За анализируемый период было выполнено 168 ахиллотомий. Для устранения деформации стоп накладывали гипсовые повязки от кончиков пальцев стопы до верхней трети бедра в согнутом коленном суставе, смена гипсовых повязок проводилась через 7–10 дней. Для полного устранения косолапости потребовалась 4–8 гипсований, сроки лечения составили от 4 до 6 нед в зависимости от ригидности деформации. Завершающим этапом после гипсования детям назначали брейсы с удержанием стопы в положении отведения 60–70° и тыльной флексии 15°. Необходимо отметить особенности ношения брейсов: в первые 4 мес лечения рекомендовано их ношение круглосуточно, далее время ношения брейсов переводили на период дневного и ночного сна.
Результаты. Изучены и оценены по 4-балльной системе результаты лечения 88 детей с врожденной косолапостью (129 стоп) в сроки от 3 мес до 3 лет: отличные результаты получены у 65 детей (73,86%), хорошие – у 11 (12,5%), удовлетворительные – у 8 (9,09%), неудовлетворительные – у 4 (4,55%)
Заключение. Метод лечения детей с врожденной косолапостью по И. Понсети можно считать золотым стандартом. Метод прост и высокоэффективен для коррекции врожденной косолапости.
Введение. Одним из наиболее распространенных инструментов для оценки функции руки является опросник Quick Disabilities of the Arm, Shoulder and Hand (QuickDASH). Чтобы рассчитать результат исследования, нужно произвести несколько математических действий: суммировать баллы, полученные в соответствии с ответами пациента, разделить полученную сумму баллов на количество ответов в опроснике, вычесть единицу, после чего полученную величину умножить на 25. Провести расчеты на бумаге непросто и затратно по времени. Поэтому многие врачи для расчета результатов исследования используют калькулятор либо производят расчеты в таблице Excel. Для упрощения процесса расчета нами разработана программа для ЭВМ «Программа для оценки функциональной декомпенсации верхних конечностей».
Цель исследования: проанализировать эффективность предлагаемой программы в сравнении с традиционными методами подсчета результатов исследования по опроснику QuickDASH.
Материал и методы. Проведен анализ 10 анкет пациентов с различной патологией кисти. Участники исследования заполняли анкеты самостоятельно после короткого объяснения задачи лечащим врачом. В подсчете результатов исследования принимали участие 10 студентов-медиков. Расчет данных, полученных в результате ответов пациентов на вопросы анкеты QuickDASH, проводился тремя способами: с помощью калькулятора, таблицы Excel и разработанной нами программы для ЭВМ. Определялось общее время, затраченное на калькуляцию всех 10 анкет и время по каждой анкете в отдельности. В качестве инструментов для расчетов студенты использовали смартфоны и стандартные приложения к электронным устройствам – калькулятор, таблицу Excel, а также программу для ЭВМ.
Результаты. Работа с электронной таблицей Excel заняла меньшее количество времени, чем работа с калькулятором, но большее, чем работа с программой для ЭВМ.
Заключение. Проведенное исследование показало эффективность предлагаемой программы для ЭВМ в сравнении с общепринятыми способами подсчета данных при работе с опросником QuickDASH.
Цель исследования: анализ результатов хирургического лечения пациентов с опухолями средостения.
Материал и методы. В период с 2006 по 2024 г. 278 пациентам (97 (34,89%) мужчин и 181 (65,11%) женщин) с опухолями средостения выполнены различные оперативные вмешательства. Возраст участников исследования варьировал от 15 до 79 лет, средний возраст составил (49, 8 ± 11,8) года. В 96 случаях были выполнены открытые вмешательства, в 182 – малоинвазивные. У 219 (78,77%) больных опухоль локализовалась в переднем средостении, у 58 (20,86%) – в заднем средостении, у одного (0,35%) – в переднем и заднем средостении.
Результаты. Полностью удалить опухоль удалось при стернотомии у 59 (21,22%) пациентов, при торакоскопии – у 134 (48,20%), торакотомии – у 18 (6,47%), двухпортовой торакоскопии – у 16 (5,75%), однопортовом доступе – у 5 (1,79%), VATS-вмешательстве – у 4 (1,43%), цервикотомии с частичной продольной стернотомией – у 2 (0,71%), при чресдвухплевральном доступе – у 1 больного (0,35%). Частичное удаление опухоли было выполнено в 16 случаях (5,75%). У 13 (4,68%) пациентов объем вмешательства был расширен из-за прорастания или врастания опухоли в сосуды корня легкого, перикард, легочную ткань или грудную стенку. Осложнения в послеоперационном периоде возникли у 20 (7,19%) пациентов. Летальность составила 2,15% (6 пациентов).
Заключение. Оперативные вмешательства у пациентов с опухолями средостения высоко эффективны, имеют низкую частоту интра- и послеоперационных осложнений и летальность. При планировании операции предпочтение следует отдавать видеоэндоскопическим методам – малотравматичным, имеющим меньшую продолжительность и высокую радикальность, сравнимую с открытыми операциями. При невозможности видеоэндоскопического вмешательства может быть рассмотрен вариант открытой операции, в том числе с расширением объема при врастании опухоли в легочную ткань, сосуды и перикард. Циторедуктивные варианты операций применимы в случаях больших размеров опухоли для уменьшения ее объема, устранения компрессии трахеи, бронхов, сосудов и проведения дальнейшего лечения (химио-, лучевая
Цель исследования: проанализировать результаты 20-летнего опыта пластики грыж пищеводного отверстия диафрагмы с помощью различных сетчатых имплантов в клинике Башкирского государственного медицинского университета.
Материал и методы. Проведено ретроспективное изучение базы данных 1516 пациентов с грыжами пищеводного отверстия диафрагмы, проходивших лечение в клинике в 2005–2024 гг., у которых коррекция включала хиатопластику с использованием сетчатого импланта. Безопасность сетчатого импланта оценивали путем регистрации осложнений, связанных с его применением. Пластику пищеводного отверстия диафрагмы считали показанной при расширении этого отверстия более 3,5 см. Проанализированы периоперационная заболеваемость, функциональные результаты и частота рецидивов, а также общая удовлетворенность пациентов результатами лечения.
Результаты. Коррекция пищеводного отверстия выполнена у 450 (29,7%) больных: диафрагмокрурорафия была осуществлена в 268 наблюдениях (17,7%), в 182 случаях (12,0%) выполнено протезирование пищеводного отверстия диафрагмы сетчатым имплантом. Детальная клинико-инструментальная оценка результатов лечения проведена у 182 пациентов с протезированием пищеводного отверстия диафрагмы сеткой. Периоперационная смертность отсутствовала. Положительный результат без послеоперационных осложнений был достигнут в 94,5% случаев. На основании анкетирования пациентов по опросникам GERD-HRQL и SF-36 и применения специальных методов исследования замыкательной функции кардии изучено качество жизни больных после операции.
Заключение. Полученные данные свидетельствуют о том, что коррекция грыж пищеводного отверстия диафрагмы с помощью аугментации нерассасывающимся сетчатым имплантом технически легко осуществима и безопасна при приемлемых показателях послеоперационных осложнений в ближайшие и отдаленные сроки наблюдения.
Введение. Анализ размеров аорты является значимым критерием в определении стратегии лечения пациентов с аневризмой, однако в современных исследованиях все чаще подчеркивается важность комплексного анализа геометрических характеристик грудной части аорты, в частности ее длины и пространственной конфигурации.
Цель исследования: проанализировать геометрические параметры грудной части аорты у пациентов с аневризмой восходящего отдела.
Материал и методы. В исследование приняли участие 70 пациентов с аневризмой восходящего отдела аорты. В зависимости от длины восходящего отдела (от аортального клапана до устья брахиоцефального ствола) больные были разделены на две группы. Первая группа (33 человека) состояла из пациентов, у которых длина аорты не превышала 111 мм (нормальная аорта), вторая группа (37 человек) была сформирована из лиц с длиной аорты, равной 111 мм и более (элонгированная аорта). Проведен сравнительный анализ клиникоинструментальных данных пациентов обеих групп.
Результаты. При сопоставимых диаметрах корня аорты, дуги и нисходящего отдела тубулярной части восходящегоотдела аорты наблюдался статистически значимо больший размер у пациентов с элонгированной аортой относительно пациентов с нормальной длиной аорты – 52 (49; 55) мм против 49 (47; 52) мм (p = 0,048). При оценке длины сегментов грудной аорты отмечено, что общая длина восходящей аорты составила 119,2 (114,0; 125,0) мм в группе пациентов с элонгированной аортой и 102,0 (89,0; 107,9) мм – с нормальной (р = 0,008). Установлено, что элонгация аорты происходит за счет как корня, так и тубулярной части восходящего отдела аорты. При этом длина дуги и нисходящего отдела грудной аорты была сопоставимой в сравниваемых группах пациентов.
Вывод. Для оценки риска развития неблагоприятных аорто-ассоциированных событий у пациентов с аневризмой восходящего отдела аорты необходимо анализировать не только диаметр аорты, но и ее длину.
Введение. Заболевания молочной железы (МЖ) включают в себя несколько типов, большинство из них не являются злокачественными. Некоторые из этих патологий достаточно безобидны и не требуют хирургического вмешательства. Другие, например, атипичная гиперплазия, эпителиоз, пограничная филлоидная карцинома и дольковая карцинома in situ (LCIS), имеют риск злокачественного перерождения и требуют тщательного наблюдения. Злокачественные поражения, включая инвазивную протоковую или дольковую карциному, протоковую карциному in situ (DCIS) и другие спорадические виды рака, в том числе злокачественную филлоидную карциному, составляют 20% от общего числа заболеваний МЖ.
Цель исследования: сравнить заболевания молочной железы в Бахрейне и России в 2022 г.
Материал и методы. Проведено ретроспективное сравнительное исследование 200 пациенток из двух стран: 100 женщин из Бахрейна (группа А) и 100 – из России (группа В). В возраст участниц исследования варьировал от 14 до 76 лет. Данные собирали с помощью предварительно структурированной анкеты. Они содержали следующие показатели: возраст пациенток, предъявляемые ими жалобы, результаты физикального обследования, латеральность, локализацию и объем поражения по данным ультразвукового исследования, классификацию по Бираду, проведенные исследования, предоперационный и послеоперационный диагноз, а также выполненные хирургические процедуры.
Результаты. Результаты были проанализированы с использованием пакета программ SPSS (версия 27). Наиболее распространенной жалобой участниц исследования было безболезненное уплотнение в МЖ: 73% случаев в группе А и 56% – в группе В. Пальпируемое уплотнение в МЖ выявлено у 74 женщин (74%) в группе А и у 87 (87%) – в группе В. Наиболее распространенной локализацией поражения являлся верхний окклюзионный отдел: 57% случаев в группе А и 56% – в группе В. Возрастной диапазон при доброкачественных состояниях в группе А составил 14–71 год, в группе В – 18–75 лет. Злокачественные состояния были диагностированы в группе А у женщин в возрасте от 36 до 76 лет, а в группе В – от 27 до 60 лет. У большинства участниц исследования были диагностированы опухоли размером менее 30 мм, при этом в группе В таких пациенток оказалось больше, чем в группе А: 92 и 74%, соответственно. В группе А регистрировалось значительно большее количество случаев с BI-RADS 2 (44%) и BI-RADS 5 (3%), в то время как в группе В наблюдалась более высокая доля случаев с BI-RADS 3 (41%) и BI-RADS 4 (42%). Ультразвуковое исследование МЖ является первым методом визуализации. Биопсию с помощью иглы использовали чаще в группе В, чем в группе А. Фиброаденома диагностировалась чаще в группе В (79%), чем в группе А (56%). Рак МЖ был диагностирован в 17 случаях в группе А и в 2 случаях в группе В.
При доброкачественных заболеваниях в группе А в большинстве случаев выполнялись хирургические вмешательства: эксцизионная биопсия – у 59% пациенток (59%), тогда как в группе В основной процедурой являлось широкое местное иссечение (86% случаев). При злокачественных заболеваниях в группе А было больше операций по удалению рака (17 случаев) по сравнению с группой В (2 случая), при этом онкопластическое широкое местное иссечение было наиболее распространенным методом в группе А (у 16 из 17 пациенток). Показатели мастэктомии были очень низкими в обеих группах – по 1 случаю в каждой.
Заключение. Таким образом, в большинстве случаев в обеих группах имели место доброкачественные заболевания молочной железы, причем наиболее часто регистрировалась фиброаденома. В большинстве наблюдений диаметр обнаруженных опухолей не превышал 30 мм. Более 40% случаев, по данным визуализации молочной железы, были оценены по шкале Bi-Rads 2 в группе А и по шкалам 3 и 4 – в группе В. Хирургические вмешательства в основном включали эксцизионную биопсию при доброкачественных новообразованиях и широкую местную резекцию – при злокачественных.
В основе представленного исследования лежал сравнительный анализ экономической эффективности монометода реконструкции молочной железы (МЖ) с применением технологии липографтинга и традиционных методов реконструкции, таких как двухэтапный метод «экспандер – имплантат» и метод TRAM-лоскута.
Проведенный сравнительный анализ свидетельствует о том, что метод реконструкции МЖ с использованием технологии липографтинга имеет сопоставимую эффективность с традиционными методами, но является статистически значимо более экономичным (p < 0,05).
В статье представлен современный взгляд на этиологию и патогенез ринофимы, описаны основные методы лечения. Представлен клинический случай успешного лечения пациента с использованием метода радиоволновой хирургии.
Цель исследования: провести сравнительный анализ клинико-инструментальных характеристик тканей молочных желез у пациенток с тубулярной деформацией I–II типа и с гипомастией для морфофункционального обоснования выбора препекторальной субфасциальной плоскости установки импланта.
Материал и методы. В проспективное когортное исследование были включены 116 пациенток: 47 женщин с тубулярной деформацией молочных желез (ТДМЖ) I–II типа и 69 – с гипомастией без признаков констрикции. Оценку состояния тканей выполняли с использованием пинч-теста, ультразвукового исследования, эластографии и визуальной шкалы эхогенности. Измеряли толщины покровных тканей молочных желез и большой грудной мышцы (БГМ), определяли эхогенность и жесткость мягких тканей.
Результаты. При ТДМЖ регистрировалась статистически значимо большая толщина покровных тканей, чем при гипомастии (9,1 ± 1,8 против (5,3 ± 1,5) мм; p < 0,001), повышенная эхогенность (4,3 ± 0,7 против (2,8 ± 0,5) балла; p < 0,001), жесткость по SWE (66,4 ± 9,2 против (39,7 ± 6,8) кПа; p < 0,001) и strain ratio (2,9 ± 0,4 против 1,7 ± 0,3; p < 0,001). У пациенток с ТДМЖ установлена также гипертрофия БГМ.
Заключение. На основании морфофункциональных особенностей покровных тканей верхнего полюса молочных желез при ТДМЖ I–II типа подтверждается состоятельность мягкотканного покрова верхнего полюса МЖ, что позволяет обосновать возможность формирования препекторального кармана без вовлечения БГМ. Такой подход снижает риск анимационных деформаций, гиперкоррекции верхнего полюса и послеоперационного болевого синдрома, обеспечивая более физиологичный и предсказуемый эстетический результат.
Рак молочной железы (МЖ) является одним из самых распространенных видов злокачественных опухолей среди женского населения не только в Российской Федерации, но и во всем мире. Поскольку основным способом лечения этой онкопатологии является хирургический, подразумевающий удаление органа, существует необходимость воссоздания последнего.
Цель исследования: сравнение данных мировых исследований, посвященных изучению качества жизни пациенток, перенесших нелоскутные реконструкции молочной железы после мастэктомии, на основании опросников Breast-Q и HADS.
Поиск литературы проводился в базах данных PubMed, eLibrary и Cyberleninka за период с 2016 по 2025 г. Для поиска применяли ключевые слова: «quality of life» (качество жизни), «breast reconstruction» (реконструкция молочной железы), «breast implant» (эндопротез молочной железы), «mesh implant» (сетчатый имплант), «Breast-Q», «HADS». Анализу подвергались оригинальные исследования, метаанализы, рандомизированные контролируемые исследования и систематические обзоры. Изучены данные о влиянии различных факторов на удовлетворенность пациенток внешним видом реконструированных МЖ и качество жизни (КЖ) в аспектах физического, психосоциального и сексуального благополучия, а также на уровень тревоги и депрессии в послеоперационном периоде.
Установлено, что применение одномоментной препекторальной реконструкции МЖ ассоциировано с более высокими показателями КЖ и низкими индексами тревоги и депрессии. Снижение показателей КЖ ассоциировано с появлением любого осложнения в послеоперационном периоде. Для определения степени влияния лучевой терапии, вида эндопротеза и его дополнительного укрытия сетчатым имплантом на показатели КЖ требуются дальнейшие исследования.
Статистика статьи
Статистика просмотров за 2026 год.
Издательство
- Издательство
- НИИ МИКРОХИРУРГИИ
- Регион
- Россия, Томск
- Почтовый адрес
- 634063, г. Томск, ул. Ивана Черных, 96
- Юр. адрес
- 634041, Томская обл, г Томск, ул Белинского, д 31/2, кв 5
- ФИО
- Байтингер Владимир Францевич (ПРЕЗИДЕНТ)
- Контактный телефон
- +7 (___) _______