Цель исследования: оценить эффективность и безопасность применения рекомбинантного интерферона гамма в комплексной терапии туберкулеза легких с лекарственной устойчивостью.
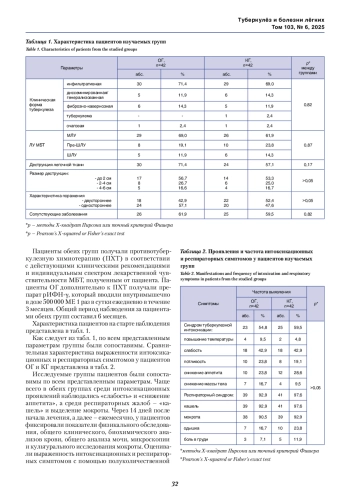
Материалы и методы. В исследование включено 84 пациента с лекарственно-устойчивым туберкулезом, путем рандомизации они разделены поровну на две группы: основную группу (ОГ) и контрольную (КГ). Пациенты обеих групп получали противотуберкулезную химиотерапию в соответствии с индивидуальной лекарственной чувствительностью микобактерий туберкулеза (МБТ). Пациенты ОГ дополнительно получали рекомбинантного интерферона гамма (рИФН-γ) (внутримышечно, в дозе 500 000 МЕ 1 раз в сутки ежедневно в течение 3 месяцев). Общий период наблюдения за пациентами составил 6 месяцев.
Результаты. В процессе лечения у пациентов обеих групп наблюдалось уменьшение клинических проявлений туберкулеза, но в ОГ это происходило быстрее. Прекращение бактериовыделения в ОГ зафиксировано в среднем через 18,6 дней лечения (микроскопия) и 16,8 дней (культуральное исследование) против 28,8 дней и 25,5 дней соответственно в КГ (p<0,05). Ко 2-му месяцу лечения положительная рентгенологическая динамика установлена у 83,3% пациентов ОГ против 30,0% в КГ (р <0,05. Через 6 месяцев лечения достигнуто рассасывание инфильтрации и очагов в легких у 92,9% пациентов в ОГ против 61,9% в КГ (р<0,05). За весь период наблюдения нежелательные явления (НЯ) зарегистрированы у 23 (54,8%) пациентов ОГ и у 17 (40,5%) пациентов КГ (р>0,05). Всего отмечены 87 НЯ: у 48 пациентов ОГ и у 39 – в КГ. У большинства пациентов встречалось по 1-2 НЯ. Наиболее часто среди НЯ встречались отклонения от нормы в лабораторных показателях. У всех пациентов ОГ переносимость препарата рИФН-γ оценивалась как отличная. Исследование показало, что применение рИФН-γ в виде 3-месячного курса дополнительно к противотуберкулезной химиотерапии может сократить сроки и улучшить эффективность лечения больных лекарственно-устойчивым туберкулезом.
Идентификаторы и классификаторы
Для повышения эффективности лечения больных туберкулезом легких с множественной лекарственной устойчивостью (МЛУ ТБ) необходим комплексный подход, учитывающий особенности как возбудителя заболевания, так и пациента. В последние годы возрос интерес к поиску адъювантов терапии, способных повысить эффективность лечения МЛУ ТБ за счет восстановления функциональной активности иммунной системы [1]. Ранее проведенные исследования различных иммуномодуляторов подтвердили, что использование интерферонов имеет клиническую перспективу [3, 5, 13].
Если у вас возникли вопросы или появились предложения по содержанию статьи, пожалуйста, направляйте их в рамках данной темы.
Список литературы
1. Баласанянц Г.С., Рузанов Д.Ю. Иммунотерапевтическая роль интерферона-γ при туберкулезе // Иммунология. - 2022. - Т. 43, №. 3. - С. 343-351.
2. Вахрушева Д.В., Красноборова С.Ю., Петрунина Е.М. Эффективность включения интерферона гамма в химиотерапию туберкулеза: экспериментальное исследование // Иммунология. - 2023. - Т. 44, №. 2. - С. 209-218.
3. Ершов Ф.И., Шульдяков А.А., Романцов М.Г., Ляпина Е.П., Соболева Л.А. Результаты и перспективы использования индукторов интерферона в лечении инфекционных болезней // Вестник Российской академии медицинских наук. - 2013. - Т. 68, № 10. - Р. 46-52.
4. Мордык А.В., Цыганкова Е.А., Пузырева Л.В., Турица А.А. Противотуберкулезный иммунитет и механизмы его формирования (обзор литературы). Дальневосточный медицинский журнал. - 2014. - № 1. - С. 126-130.
5. Суханов Д.С. Иммунотропная терапия туберкулезной инфекции // Терапевтический архив. - 2013. - № 3. URL: https://cyberleninka.ru/article/n/immunotropnaya-terapiya-tuberkuleznoy-infektsii.
6. Abate G., Hoft D.F. Immunotherapy for tuberculosis: future prospects // Immunotargets Ther. - 2016. - № 5. - Р. 37-45. DOI: 10.2147/ITT.S81892
7. Common Terminology Criteria for Adverse Events (CTCAE) v5.0 Publish Date: November 27, 2017. Available at: http://ctep.cancer.gov.
8. Condos R., Rom WN & Schluger NW. Treatment of multidrug-resistant pulmonary tuberculosis with interferon-gamma via aerosol // Lancet. - 1997. - № 349. - P.1513-1515.
9. Davoudi S., Rasoolinegad M., Younesian M., Hajiabdolbaghi M., Soudbakhsh A., Jafari S., EmadiKouchak H., Mehrpouya M., Lotfi H. CD4+ cell counts in patients with different clinical manifestations of tuberculosis // Braz J Infect Dis. - 2008. - Vol. 12, № 6. - Р.483-486.
10. Dawson R., Condos R., Tse D., Huie M.L., Ress S., Tseng C.H., Brauns C., Weiden M., Hoshino Y., Bateman E., Rom W.N. Immunomodulation with recombinant interferon-gamma1b in pulmonary tuberculosis // PLoS One. - 2009. - Vol.4, № 9. - Р.e6984.
11. Ehrt S., Schnappinger D., Bekiranov S., Drenkow J., Shi S., Gingeras T.R., Gaasterland T., Schoolnik G., Nathan C. Reprogramming of the macrophage transcriptome in response to interferon-gamma and Mycobacterium tuberculosis: signaling roles of nitric oxide synthase-2 and phagocyte oxidase // J. Exp. Med. - 2001. - № 194. - Р. 1123-1140. DOI: 10.1084/jem.194.8.1123
12. Ghanavi J., Farnia P., Farnia P., Velayati A.A. The role of interferon-gamma and interferon-gamma receptor in tuberculosis and nontuberculous mycobacterial infections // Int. J. Mycobacteriol. - 2021. - Vol. 10, № 4. - Р. 349-357.
13. Giosuè S., Casarini M., Ameglio F., Zangrilli P., Palla M., Altieri A.M., Bisetti A. Aerosolized interferon-alpha treatment in patients with multi-drug-resistant pulmonary tuberculosis // Eur Cytokine Netw. - 2000. - Vol. 11, № 1. - Р. 99-104.
14. Koh W.J., Kwon O.J., Suh G.Y., Chung M.P., Kim H., Lee N.Y., Kim T.S., Lee K.S. Six-month therapy with aerosolized interferon-gamma for refractory multidrug-resistant pulmonary tuberculosis // J Korean Med Sci. - 2004. - Vol. 19, № 2. -Р.167-171.
15. Kononova T.E., Urazova O.I., Novitskiĭ V.V., Churina E.G. T-lymphocyte-helper type 17 mediated regulation of antibacterial (antituberculosis) immunity // Mol Biol (Mosk). - 2013. - Vol. 47, № 6. - Р. 883-890.
16. Maslennikov A.A., Obolonkova N.I. Efficacy of Ingaron in the complex therapy of patients with destructive bacterial excretion of pulmonary tuberculosis // Network journal “Scientific result”. The series “Medicine and Pharmacy”. - 2016. - № 7. - Р.10-16.
17. Ma Z., Li S., Liu Y., Li C., Wang X., Tang X., Dong R., Zheng S., Wang L. Serum lymphocytes and cytokines: diagnostic value and influence on the immune status in patients with pulmonary tuberculosis // J Bras Pneumol. - 2023. - Vol. 49, № 5. - Р. e20230154.
18. Schoenborn J.R., Wilson C.B. Regulation of interferon-gamma during innate and adaptive immune responses //Adv Immunol. - 2007. - № 96. - Р.41-101.
19. Suárez-Méndez R., García-García I., Fernández-Olivera N., Valdés-Quintana M., Milanés-Virelles M.T., Carbonell D., Machado-Molina D., Valenzuela-Silva C.M., López-Saura P. Adjuvant interferon gamma in patients with drug-resistant pulmonary tuberculosis: a pilot study // BMC Infect Dis. - 2004. - № 4. - Р. 44.
20. Vasileva I. A., Samoilova A.G., Abramchenko A.V., Avdeev V.V., Vinokurov A.S., Romanova M.Y., Kayukova S.I. Efficacy of Interferon-γ (Ingaron) Against Tuberculosis in BALB/c Mouse Mode. 2024. Available at: https://www.preprints.org/manuscript/202406.1950.
21. Yin Y., Qin J., Dai Y., Zeng F., Pei H., Wang J. The CD4+/CD8+ Ratio in Pulmonary Tuberculosis: Systematic and Meta-Analysis Article // Iran J Public Health. - 2015. - Vol. 44, № 2. - Р.185-193.
Выпуск
Другие статьи выпуска
Фармакогенетическое тестирование – наиболее перспективный инструмент персонализированной медицины, направленный на повышение эффективности и безопасности лечения, особенно у сложных коморбидных пациентов. Проведен анализ 122 публикаций, посвященных теоретическим и прикладным аспектам применения фармакогенетического тестирования при лечении больных туберкулезом. Рассмотрена роль генетических полиморфизмов в ответе на лечение, представлены данные о белках, участвующих в процессах фармакокинетики и фармакодинамики основных противотуберкулезных препаратов, и кодирующих эти белки генах. Проанализирован перечень наиболее значимых маркеров, связанных с риском нежелательных реакций при лечении лекарственно-чувствительного и лекарственно-устойчивого туберкулеза, охарактеризованы перспективы их применения в клинической практике. В списке литературы отражены 56 ключевых публикаций, на которые имеются ссылки в тексте.
Одним из перспективных направлений в диагностике туберкулеза являются трегалозные зонды, способные селективно проникать в Mycobacterium tuberculosis (МБT). При этом зонды генерируют флуоресцентный сигнал, позволяя проводить таким образцом детекцию. Для анализа современного состояния и перспектив применения трегалозных зондов, как нового подхода к экспресс-диагностике Mycobacterium tuberculosis, проведен обзор научной литературы. Рассмотрены основные типы зондов: флуорогенные, построенные по схеме «флуорофор-тушитель» и фотоактивируемые. Трегалозные зонды обеспечивают селективную детекцию МБT за счет специфического поглощения трегалозы, встраивания в клеточную стенку и последующей активации флуоресценции. Зонды позволяют обнаруживать МБT в образцах мокроты без сложной пробоподготовки и этапов отмывки. Методика позволяет дифференцировать жизнеспособные и нежизнеспособные клетки МБT, а также может применяться для тестирования их лекарственной чувствительности.
В последние годы возрос интерес к фаговым технологиям как к перспективным методам быстрого определения спектра лекарственной чувствительности бактерий, в том числе Mycobacterium tuberculosis. Микобактериофаги способны специфически инфицировать M. tuberculosis, что дает возможность разработки новых эффективных, экономичных диагностических тестов, а также принципиально новых лекарственных препаратов для лечения туберкулеза. Проанализированы 27 источников, описывающие основные методы, используемые для определения спектра лекарственной чувствительности M. tuberculosis с помощью микобактериофагов. Преимуществом этих методов являются: быстрота (получение результатов за 24-96 часов с момента начала анализа); специфичность (основаны на строгом круге хозяев фага). Это позволяет в короткие сроки выявлять наличие возбудителя туберкулеза и его лекарственную чувствительность к противотуберкулезным препаратам.
Туберкулез женских половых органов – болезнь преимущественно репродуктивного возраста, реже заболевание развивается у женщин в постменопаузе. Приведен клинический случай диагностики туберкулеза половых органов у женщины 72 лет. У нее ультразвуковое исследование живота выявило серозометру и жидкостные образования в правом яичнике. Гистологическое исследование соскоба стенок и шейки матки диагностической информации не дало. При лапароскопии обнаружили выраженные спайки и инкапсулированный очаг. Гистологическое исследование операционного материала подтвердило туберкулез.
Представлен клинический случай успешного лечения у пациентки 13 лет посттуберкулезного стеноза левого главного бронха 3-4 степени с помощью самофиксирующегося эндопротеза. В результате химиотерапии туберкулеза продолжительностью 24 месяца, и эндопротезирования продолжительностью 18 месяцев удалось вылечить туберкулез легких и бронхов, восстановить функцию ЛГБ, избежать органоуносящей операции у ребенка. Метод лечения с помощью самофиксирующихся эндопротезов во фтизиатрической детской практике применен впервые.
Цель исследования: изучить у больных ВИЧ-инфекцией функциональные исходы экстраплевральной торакопластики по поводу деструктивного туберкулеза через 6 месяцев после операции.
Материалы и методы. Ретроспективно было сформированы две группы пациентов, перенесших экстраплевральную торакопластику (ЭПТ) по поводу деструктивного туберкулеза легких: в основную группу (ОГ) вошли 49 пациентов с ВИЧ-инфекцией, в группу сравнения (ГС) были выбраны 49 пациентов без ВИЧ-инфекции, сопоставимые с ОГ по возрасту, полу, распространенности туберкулеза легких. У пациентов обеих групп были оценены следующие показатели: динамика одышки, жизненная емкость легких (ЖЕЛ), объем форсированного выдоха за первую секунду (ОФВ1), индекс Тиффно, показатели капиллярного легочного кровотока (КЛК).
Результаты. В группе ОГ операция экстраплевральной торакопластики способствовала ликвидации полости деструкции к сроку 6 месяцев у 30,6% (15/49 пациентов), прекращению бактериовыделения у 46,9% (23/49 пациентов). Эти показатели значимо не отличались от таковых у пациентов группы сравнения (с ВИЧ-отрицательным статусом). Ухудшение результатов спирометрии зафиксировано у 28,3±14,6% пациентов в ОГ и у 29,5±14,6% в ГС, p>0,05; КЛК сохранялся на дооперационном уровне в обеих группах. У 14 (28,6%) больных ОГ при недостаточном эффекте ЭПТ (сохранение полостей распада и бактериовыделения) выявлено существенное уменьшение степени одышки после операции без значимых изменений дооперационных показателей спирометрии. Это позволяет считать операцию ЭПТ безопасной в функциональном отношении.
Цель исследования: оценка применения двухэтапного эндопротезирования при лечении деструктивной формы септического гонита туберкулезной и неспецифической этиологии, включая ВИЧ-позитивных пациентов.
Материалы и методы. В исследование вошли 15 пациентов с деструктивной формой септического гонита как неспецифической или/и туберкулезной этиологии, которым проводилось хирургическое лечение. У 7/15 (46,67%) пациентов была туберкулезная этиология заболевания, у 8 (53,33%) – неспецифическая, ВИЧ-позитивный статус имели 5/15 (33,33%) пациентов. У пациентов планировалось двухэтапное эндопротезирование с использованием цементных артикулирующих спейсеров, насыщенных антимикробными препаратами по лекарственной чувствительности возбудителя. У 10 пациентов (66,67%) выполнен полный цикл двухэтапного эндопротезирования, в 5 случаях (33,33%) – только первый этап.
Результаты. Во всех 15 случаях у пациентов получена стойкая эрадикация инфекции. У 10 пациентов, закончивших весь цикл хирургического лечения, по шкале KSS получено статистически значимое улучшение показателей с 35,4 ± 15,4 до 78,2 ± 15,1 (p<0,05), сроки наблюдения – от 1 года до 14 лет. Не отмечено значимого влияния ВИЧ-инфекции на полученные результаты лечения.
Цель исследования: сравнительная оценка гепатотоксичности комбинаций противотуберкулезных препаратов (ПТП), в том числе рекомендуемых для коротких курсов химиотерапии, анализ протекторных свойств семакса и аскорбигена.
Материалы и методы. Исследование состояло из 2-х экспериментов, которые различались по комбинации ПТП и препарату сопровождения. В 1-м эксперименте крысы опытных групп получали Mxf Lzd Pto Cs Z и Mxf Lzd Pto Cs Z + семакс; во 2-м эксперименте – Mxf Lzd Pto Bdq Cfz и Mxf Lzd Pto Bdq Cfz + аскорбиген. Крысы контрольных групп получали перорально 1%-ный крахмальный гель. Длительность введения составила 14 дней во всех группах. Гепатотоксичность оценивали по биохимическим показателям и патоморфологическим критериям.
Результаты. У крыс, получавших Mxf Lzd Pto Cs Z, определяли статистически значимое повышение активности трансаминаз и содержания общего билирубина, выраженные изменения ткани печени по сравнению с контрольной группой. У крыс, получавших Mxf Lzd Pto Bdq Cfz, на фоне повышения активности трансаминаз патоморфологические изменения печени были менее выражены. Применение семакса и аскорбигена способствовало нормализации ферментативной активности и снижению повреждения ткани печени. Показано, что токсикомодифицирующие свойства аскорбигена более выражены, однако гепатопротекторный потенциал семакса проявился при более глубоких структурных нарушениях печени.
Цель исследования: изучить факторы, влияющие на результаты лечения у впервые выявленных больных туберкулезом из коренных малочисленных народов Севера (КМНС), проживающих в Ямало-Ненецком автономном округе (ЯНАО).
Материалы и методы. Проведено ретроспективное когортное исследование результатов лечения впервые выявленных пациентов, зарегистрированных для лечения по режимам лекарственно-чувствительного туберкулеза в ЯНАО за 2010- 2022 гг. Выполнен факторный анализ предикторов неблагоприятного исхода химиотерапии у пациентов из числа КМНС.
Результаты. Среди пациентов из числа КМНС отмечается более низкая частота успешного лечения (58,79%) туберкулеза, чем среди некоренных постоянных жителей ЯНАО (68,45%; p=0,001) за счет высокой частоты последующего выявления лекарственной устойчивости возбудителя и перевода на соответствующий режим лечения (p<0,0001), высокой частоты неудач курса химиотерапии (p=0,001) у ряда пациентов, ассоциированной с наличием алкогольной зависимости (ОШ=2,80; p=0,045), позднего выявления туберкулеза (p=0,01). Для данной категории населения целесообразно обсудить ежегодную частоту флюорографического обследования на туберкулез.
Цель исследования: определить ранние факторы неблагоприятного течения сочетания ВИЧ-инфекции и туберкулеза для совершенствования подходов к лечению таких пациентов.
Материалы и методы. В исследование включено 105 пациентов с ВИЧ-инфекцией, у которых впервые выявлен туберкулез и обнаружены в биологическом материале ДНК М. tuberculosis (МБТ) молекулярно-генетическим методом. Пациенты разделены на две группы: с благоприятным течением сочетания ВИЧ-инфекции и ТБ (78 человек) и неблагоприятным течением (27 человек).
Результаты. Определены значимые факторы, влияющие на течение сочетания ВИЧ-инфекции и ТБ и легкодоступные у каждого пациента (уровни лейкоцитов (х), гемоглобина (у), альбумина (z), железа (w). Была построена дискриминантная модель, представляющая формулу D= -8,263-0,110x+0,012y+0,197z+0,024w. Точность модели 83,3%. Если полученный показатель D ≥ -0,301, то пациент имеет низкий риск неблагоприятного течения сочетанного заболевания, в случае D< -0,301, пациент имеет высокий риск неблагоприятного течения сочетанного заболевания ВИЧ-инфекции и туберкулеза. При неблагоприятном прогнозе выполнение расширенного молекулярно-генетического анализа лекарственной устойчивости МБТ позволит подобрать актуальную схему лечения ТБ. При отсутствии данных по МБТ следует использовать режимы лечения лекарственно-устойчивого туберкулеза.
Цель исследования: оценка возможности современных методов тестирования устойчивости к рифампицину в выявлении гетерорезистентности культур Mycobacterium tuberculosis.
Материалы и методы. Искусственно созданы смеси чувствительного (H37Rv) и устойчивого (штамм 5521 с ШЛУ, с мутацией rpoB Ser531Leu) штаммов МБТ в пропорциях от 0% до 100%. Для тестирования устойчивости к рифампицину использованы фенотипические методы (BACTEC MGIT 960, метод пропорций на среде Миддлбрук 7H10) и молекулярно-генетические тесты (ТБ-ТЕСТ, Амплитуб-МЛУ-РВ, АмплиТест МБТ-Резист I).
Результаты. Фенотипические методы выявили устойчивость к рифампицину при 1% резистентных клеток в смеси. Молекулярно-генетические методы показали вариабельный порог детекции: 5% (АмплиТест МБТ-Резист I), 20% (ТБ-ТЕСТ), 30% (Амплитуб-МЛУ-РВ). Показана возможность повышения чувствительности отечественных молекулярно-генетических тест-систем путем совершенствования программ интерпретации данных ПЦР, а также необходимость разработки алгоритмов диагностики ЛЧ МБТ с учетом ограничений используемых методов.
Цель исследования: сравнить эффективность и безопасность лечения туберкулеза с лекарственной чувствительностью при применении четырехмесячного и шестимесячного режимов химиотерапии.
Материалы и методы. В период с октября 2023 по август 2025 гг. проведено многоцентровое когортное исследование по лечению лекарственно-чувствительного туберкулеза с применением короткого (четырехмесячного) режима (группа КР) химиотерапии (ХТ) по схеме: рифапентин (900 мг в сутки), изониазид, пиразинамид, левофлоксацин в интенсивной фазе в течение двух месяцев и рифапентин (900 мг в сутки), изониазид и пиразинамид в фазе продолжения. Группу сравнения (СР) составили пациенты, получавшие в этот период шестимесячный режим ХТ лекарственно-чувствительного туберкулеза. Результаты эффективности оценивались по прекращению бактериовыделения и клинико-рентгенологической динамике.
Результаты. Эффективный результат лечения достигнут у 92,0% (46/50) пациентов в группе КР против 76,6% (46/60) в группе СР (p=0,038). Прекращение бактериовыделения по микроскопии к концу ХТ зарегистрировано у 96,0% (48/50) и 76,7% (46/60) соответственно (p=0,005); культурально – у 94,0% (47/50) и у 73,3% (44/60) (p=0,004). Общая частота нежелательных реакций была ниже в группе КР (57,7%) против 74,6% в группе СР, p=0,045.
Статистика статьи
Статистика просмотров за 2026 год.
Издательство
- Издательство
- РОФ
- Регион
- Россия, Москва
- Почтовый адрес
- 127473, г Москва, р-н Марьина роща, ул Достоевского, д 4
- Юр. адрес
- 127473, г Москва, р-н Марьина роща, ул Достоевского, д 4
- ФИО
- Васильева Ирина Анатольевна (ПРЕЗИДЕНТ)
- Контактный телефон
- +7 (___) _______
- Сайт
- https://rof-tb.ru/