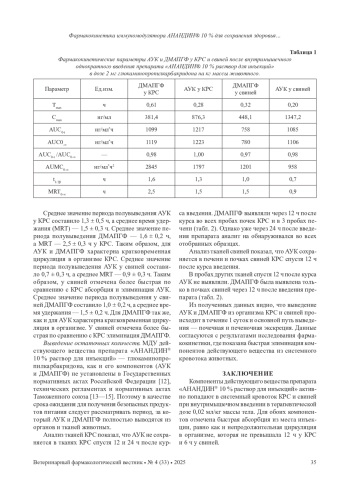
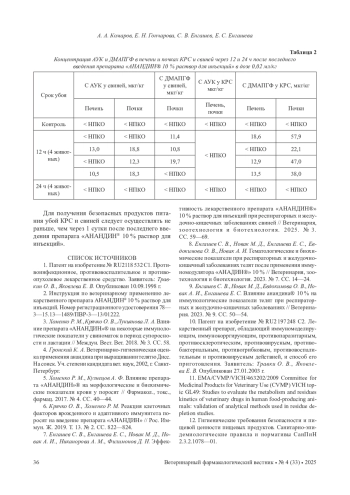
Действующее вещество препарата «АНАНДИН® 10 % раствор для инъекций» - глюкаминопропилкарбакридон, являющееся комплексным соединением, состоящим из N-акридонуксусной кислоты (АУК) и диметиламинопропилглюкофуранозы (ДМАПГФ). При исследовании фармакокинетики определяли оба компонента. По результатам экспериментов установлено, что АУК и ДМАПГФ активно проникают в системный кровоток КРС и свиней после внутримышечного введения в терапевтической дозе0,02 мл/кг массы тела, распределяясь по всему организму. Для обоих компонентов отмечена быстрая абсорбция из места инъекции и циркуляция в организме свиней в течение 6 ч и 12 ч у КРС. Предлагаемаядозировка и внутримышечный способ введения препарата «АНАНДИН® 10 % раствор для инъекций»обеспечивают хорошую абсорбцию и распределение компонентов действующего вещества в организмеКРС и свиней. По результатам анализа проб органов и тканей КРС и свиней на остаточное содержание АУК и ДМАГПФустановлено, что для получения безопасных продуктов питания убой КРС и свиней следует осуществлятьчерез 1 сутки после курсового внутримышечного применения препарата «АНАНДИН® 10 % раствор дляинъекций».
Идентификаторы и классификаторы
- SCI
- Ветеринария
Для кормления применяли рацион, составленный с учетом возраста и включающий комбикорм для свиней СПК‑5. В помещении использовалось искусственное освещение. Доступ к воде не огра‑ ничивали. Температура в помещении находилась в промежутке 16—27 °C, относительная влажность воздуха — 45—70 %.
Если у вас возникли вопросы или появились предложения по содержанию статьи, пожалуйста, направляйте их в рамках данной темы.
Список литературы
1. Патент на изобретение № RU2118 532 C1. Противоинфекционное, противовоспалительное и противоопухолевое лекарственное средство. Заявитель: Травкин О. В., Яковлева Е. В. Опубликован 10.09.1998 г.
2. Инструкция по ветеринарному применению лекарственного препарата АНАНДИН® 10 % раствор для инъекций. Номер регистрационного удостоверения 78- 3-15.13-1489/ПВР-3-13/01222.
3. Хоменко Р. М., Крячко О. В., Лукьянова Л. А. Влияние препарата “АНАНДИН”® на некоторые иммунологические показатели у свиноматок в период супоросности и лактации // Междун. Вест. Вет. 2018. № 3. СС. 58.
4. Гронский К. А. Ветеринарно-гигиеническая оценка применения анандина при выращивании телятю Дисс. На соиск. Уч. степени кандидата вет. наук, 2002, г. Санкт-Петербург. EDN: NMCMTV
5. Хоменко Р. М., Кузнецов А. Ф. Влияние препарата “АНАНДИН”® на морфологические и биохимические показатели крови у поросят // Фармакол., токс., фармац. 2017. № 4. СС. 40-44.
6. Крячко О. В., Хоменко Р. М. Реакция клеточных факторов врожденного и адаптивного иммунитета поросят на введение препарата “АНАНДИН” // Рос. Иммун. Ж. 2019. Т. 13. № 2. СС. 822-824.
7. Енгашев С. В., Енгашева Е. С., Новак М. Д., Новак А. И., Никанорова А. М., Филимонов Д. Н. Эффективность лекарственного препарата “АНАНДИН®”% раствор для инъекций при респираторных и желудочно-кишечных заболеваниях свиней // Ветеринария, зоотехнология и биотехнология. 2025. № 3. СС. 59-69.
8. Енгашев С. В., Новак М. Д., Енгашева Е. С., Евдокимова О. В., Новак А. И. Гематологические и биохимические показатели при респираторных и желудочно-кишечный заболеваниях телят после применения иммуномодулятора “АНАДИН®” 10 % // Ветеринария, зоотехнология и биотехнология. 2023. № 7. СС. 14-24.
9. Енгашев С. В., Новак М. Д., Евдокимова О. В., Новак А. И., Енгашева Е. С. Влияние анандина® 10 % на иммунологические показатели телят при респираторных и желудочно-кишечных заболеваниях // Ветеринария. 2023. № 9. СС. 50-54.
10. Патент на изобретение № RU2 197 248 С2. Лекарственный препарат, обладающий иммуномоделирующим, иммунокорргирующим, противопаразитарным, противосклеротическим, противовирусным, противобактериальным, противогрибковым, противовоспалительным и противовирусным действией, и способ его приготовления. Заявитель: Травки О. В., Яковлева Е. В. Опубликован 27.01.2003 г.
11. EMA/CVMP/VICH/463202/2009 Committee for Medicinal Products for Veterinary Use (CVMP) VICH topic GL49: Studies to evaluate the metabolism and residues kinetics of veterinary drugs in human food-producing animals: validation of analytical methods used in residue depletion studies.
12. Гигиенические требования безопасности и пищевой ценности пищевых продуктов. Санитарно-эпидемиологические правила и нормативы СанПиН 2.3.2.1078-01.
13. ТР ТС 034/2013 Технический регламент Таможенного союза “О безопасности мяса и мясной продукции”.
14. Единые санитарно-эпидемиологические и гигиенические требования к продукции (товарам). подлежащей санитарно - эпидемиологическому надзору (контролю) (с изменениями на 21 мая 2019 года), утв. Решением Комиссии таможенного союза от 28 мая 2010 года N299, раздел 15.
15. Решение Коллегии Евразийской экономической комиссии от 13 февраля 2018 г. № 28 “О максимально допустимых уровнях остатков ветеринарных лекарственных средств (фармакологически активных веществ), которые могут содержаться в непереработанной пищевой продукции животного происхождения, в том числе в сырье, и методиках их определения”.
Выпуск
Другие статьи выпуска
Спермиогенез у баранов включает четыре фазы: 1 - фазу Гольджи; 2 - фазу колпачка; 3 -фазу акросомы; 4 - фазу созревания. В фазу Гольджи входят первые три этапа спермиогенеза (1-3). В цитоплазме молодых сперматид с помощью комплекса Гольджи формируется проакросомический пузырек, в котором накапливается ШИК - положительный материал в виде крупной акросомальной гранулы. Следующие четыре этапа спермиогенеза (4-7) составляют фазу колпачка. Акросомический пузырек располагается на поверхности оболочки ядра в виде колпачка, покрывая её одну третью часть. К концу фазы колпачка акросомальная структура покрывает половину поверхности ядра. Ядро приобретает овальную форму и смещается к переднему полюсу клетки. В период фазы акросомы (8-11 этапы спермиогенеза) акросомальная структура удлиняется, формируется акросомический конус с острым концом. В течение последней фазы созревания (12-17 этапы) сперматиды с удлиненной акросомой приближаются к ядру клеток Сертоли. Последние гипертрофируются, располагаются перпендикулярно базальной мембранеи мигрируют ближе к центру семенного канальца. К концу фазы созревания исчезает акросомический конус, сперматиды превращаются в сперматозоиды, которые перемещаются в канал придатка семенника.
Патологии печени у крупного рогатого скота сопровождаются метаболическими и иммунными нарушениями, отражающимися на составе крови. Целью работы было оценить изменения морфологических показателей крови и интегральных лейкоцитарных индексов у коров при патологиях печени. Исследование проводили на 100 коровах. Биохимические показатели в сыворотке крови измеряли с помощью автоматиче ского анализатора «Chem Well-2910 Combi» (Awareness Technology, США). Ретроспективно сформировали пять групп по 10 голов в каждой: 1 - здоровые (без патологий печени);2 - легкая степень цитолиза; 3 - средняя степень цитолиза; 4 - легкая степень холестаза; 5 - средняя степень холестаза. Гематологические показатели измеряли с помощью автоматического анализатора «Abacus Junior Vet» (Diatron, Австрия). На основе лейкоцитарной формулы рассчитывали интегральные лейкоцитарные индексы: интоксикации (в модификациях ЛИИ Рейса), сдвига лейкоцитов крови (ИСЛК), лимфоцитарно - гранулоцитарный (ИЛГ), соотношения нейтрофилов и моноцитов (ИСНМ), соотношения лимфоцитов и моноцитов (ИСЛМ) и Кребса (ИК). Установлено, что содержание эритроцитов, тромбоцитов и лейкоцитов в крови больных и здоровых коров статистически значимо не различались (р > 0,05). У животных с легкой степенью цитолиза выявили снижение относительного содержания моноцитов на 23,3 % (р < 0,05), со средней - увеличение уровня сегментоядерных нейтрофилов на 37,5 % (р < 0,05), соответственно по сравнению со здоровыми особями. При прогрессировании цитолиза у коров отмечали тенденцию к уменьшению ИЛГ и увеличению ИК, ИСЛК, ИСЛМ, ИСНМ и ЛИИ Рейса. У животных с легкой и средней степенью холестаза наблюдали повышение уровня сегментоядерных нейтрофилов на 15,6 и 21,9 % (р < 0,05) при отсутствии изменений и снижении содержания лимфоцитов на 20,2 % (р < 0,05), соответственно, по сравнению со здоровыми особями. Изменения в лейкоцитарной формуле таких коров сопровождались уменьшением ИЛГ на 19,9 и 39,0 % (р < 0,05) и повышением ИСНМ на 13,2 и 17,6 % (р < 0,05), ИК - на 19,3 и 57,5 % (р < 0,05), ИСЛК - на 20,5 и 63,4 % (р < 0,05), ЛИИ Рейса - на 27,2и 25,9 % (р < 0,05), соответственно, ИСЛМ при легкой степени холестаза оставался без существенных изменений, а при средней - повышался на 23,7 % (р < 0,05) по сравнению со здоровыми. Результаты исследования подтверждают возможность использования интегральных лейкоцитарных индексов для дифференциальной диагностики, оценки тяжести и прогнозирования течения заболеваний печени у коров.
В статье представлены результаты изучения влияния кормовой добавки «Лозекорм» на клеточный иммунитет кур - несушек. Для оценки функционального состояния клеточного звена иммунитета применялась реакция бласттрансформации лимфоцитов (РБТЛ) с расчетом индекса стимуляции пролиферации (ИСП). Установлено, что введение «Лозекорм» в рацион кур - несушек способствует стимулированию пролиферативной активности мононуклеарных клеток периферической крови, что подтверждает активизацию Т - клеточного иммунного ответа. Повышение иммунного статуса свидетельствует об эффективности применения добавки «Лозекорм» для коррекции иммунологической реактивности у птицы.
В статье приведены материалы по распространению мастита у коров. Установлено, что субклиническая форма мастита у коров является наиболее распространенной, которая диагностирована у 34,5 % обследованных коров при частоте поражения 12,6 % долей. Интенсивность поражения долей молочнойжелезы субклиническим маститом не имела значительной вариабельности в связи с возрастом коров, периодом лактации, но была выражена сезонность. При сопоставлении частоты заболевания передних и задних долей молочной железы коров субклиническим маститом, установили незначительное преимущественное поражение задних долей. На частоту заболевания коров субклиническим маститом при машинном доении существенное влияние оказывает величина, форма и расположение сосков.
Заворот большой ободочной кишки у лошадей является одной из самых опасных и тяжелых форм и заболеваний желудочно - кишечного тракта. Заболевание развивается стремительно, требует немедленной госпитализации в профильную клинику и оперативного лечения. Стопроцентная летальность при отсутствии оперативного лечения, а также необходимость начать операцию как можно раньше делают актуальной проблему ранней диагностики заболеваний большой ободочной кишки, требующих хирургического вмешательства. Зачастую невыраженные клинические признаки в начале развития болезни, отсутствие постоянного контроля за животным и слабая информированность по данной проблеме владельцев животных приводят к фатальным последствиям. Развиваются тяжелые вторичные изменения в виде эндотоксемия, сепсиса, перитонита, дыхательной и сердечно - сосудистой недостаточности. Все вышеперечисленное значительно затрудняет как проведение самой операции, так и постоперативное ведение пациентов и приводит к невозможности проведения какого - либо лечения и как следствие, гибели животного или необходимости эвтаназии. Целью данной работы являлось изучение особенностей диагностики острых заболеваний толстого отдела кишечника лошадей, способствующим наиболее эффективному лечению и минимизации случаев летального исхода.
Данное исследование посвящено анализу потенциала азитромицина - 15-членного макролида, обладающего широким спектром антимикробных и иммуномодулирующих свойств, - в лечении цитозооноза у кошек. В работе рассмотрены структурные особенности препарата, его механизмы действияи фармакокинетические преимущества. Особое внимание уделено возможности использования азитромицина в ветеринарии, в частности, в комплексной терапии паразитарных заболеваний, таких как цитозооноз, вызываемый паразитом Cytauxzoon felis. Проанализированы существующие схемы лечения, их эффективность и сравнительные показатели выживаемости животных. Полученные данные свидетельствуют о высокой эффективности комбинации азитромицина с противомалярийными препаратами, что значительно снижает уровень смертности. Исследование подчеркивает актуальность дальнейших клинических и экспериментальных работ по внедрению азитромицина в ветеринарную практику для повышения эффективности борьбы с опасными паразитарными инфекциями у домашних животных.
В статье представлены результаты сравнительнойоценки измененийразмеров фолликулов в яичниках, выполненной с помощью клиническо - эхографического исследования, уровня секреции эстрадиола 17-β, определяемого методом ИФА в сыворотке крови, а также ультрасонографического контроля времени овуляции после действия прогестеронсодержащих внутривлагалищных имплантов с добавлением разных дозировок мелатонина, применяемых в составе схемы синхронизации половой охоты у молочных коров. В группах, где применялись импланты с мелатонином в дозировках 500 и 700 мг, размер предовуляторных фолликулов был на 8,0 и 10,1 % больше по сравнению с контролем. Также, биологическая активность данного пептида повлияла на функцию гранулёзных клеток, на что указывает повышение секреции эстрадиола на 15,0 и 33,7 % относительно группы контроля, в гормонально индуцированную стадию полового возбуждения. Следствием образования более крупных фолликулов и оптимизации стероидогенеза в яичниках стало своевременное наступление овуляции в ответ на инъекцию гонадолиберина.
В настоящее время научные исследования, связанные с разработкой поликомпонентных пробиотиков, состав которых дополнен фитобиотическими или минеральными веществами, относят к актуальным направлениям фармакологии. Кормовая добавка сиолакт представляет собой комплекс лакто - и бифидобактерий с природным алюмосиликатным минералом. Цель работы состояла в оценке влияния сиолакта на продуктивность и биохимические показатели крови цыплят - бройлеров. Исследования проведены на 60 цыплятах - бройлерах кросса Arbor Acres, из которых по принципу параналогов было сформировано две группы по 30 особей (опытная и контрольная) в каждой. Цыплята из опытной группы с 5 по 42 дни жизни получали кормовую добавку сиолакт (0,1 % от массы комбикорма). Контрольная группа находиласьна основном рационе. В результате проведенных исследований установлено, что сиолакт оказывает положительное влияние на метаболизм птицы, проявляющееся улучшением показателей белкового и углеводного обменов, а также маркеров состояния печени. Введение в рацион цыплят кормовой добавки способствует увеличению приростов массы тела птицы при разнице с контролем в 4,57 % (p ≤ 0,05) к 42 дню жизни, а также повышает сохранность поголовья на 6,7 %.
В статье приведены результаты по оценке эффективности средства Эковет-А в профилактике мастита у коров. Эковет-А представляет собой электрохимически активированный раствор хлоркислородных и гидропероксидных соединений. Для исследований сформировали три группы (две опытныеи одну контрольную) условно здоровых лакирующих коров по 20 голов в каждой. В схему обработки вымени коров перед доением включали: в 1 опытной группе средство Эковет-А; во 2 опытной группе - средство для обработки вымени на основе молочной кислоты. Дезинфицирующие средства применяли в течение месяца методом окунания сосков в невозвратный стаканчик на 30 секунд, в контрольной группе использовали воду. В результате проведенных исследований установлено, что за месячный периодприменения дезинфицирующих средств в преддоильной обработке коров в опытных группах количествотрещин сосков вымени и случаев мастита относительно контрольного поголовья снизилось на 10-30 %, с наилучшим результатом в 1 опытной группе. При применении средства Эковет-А относительно контроля в молоке коров зарегистрировано снижение количества соматических клеток - в 1,8 раз и КМАФАнМ -в 1,5 раза. Таким образом, для профилактики мастита у коров средство Эковет-А может эффективно использоваться в схеме обработки вымени перед доением.
Адъюванты являются критическим компонентом большинства ветеринарных вакцин, обеспечивая усиление иммунного ответа организма на вакцинный антиген. Приблизительно 87 % коммерческих инактивированных вакцин для животных содержат в своем составе один тип адъюванта, наиболеераспространёнными из которых являются минеральные соли алюминия (48 %), масляные эмульсии (20 %) и сапонины. В настоящей работе систематизирован современный опыт применения пяти основных классов адъювантов: неорганических минеральных соединений, органических масляных композиций, растительных сапонинов, бактериальных производных и наноструктурированных материалов. Каждый класс обладает специфическими механизмами действия, влияющими на формирование гуморального и клеточного иммунитета у различных видов сельскохозяйственных животных. Однако применение адъювантов требует соблюдения баланса между иммуногенностью и реактогенностью. Традиционные адъюванты могут вызывать локальные реакции (гранулёмы, абсцессы) и системные эффекты (лихорадку, снижение продуктивности) особенно у чувствительных видов. Перспективные направления включают разработку биоразлагаемых наносистем, синтетических аналогов растительных сапонинов и комбинированных адъювантных систем, обеспечивающих повышенную специфичность к различным видам животных. Будущие адъюванты должны обеспечивать целенаправленную активацию требуемых компонентов иммунитета приминимизации побочных эффектов, что откроет новые возможности для профилактики и эрадикации опасных инфекционных заболеваний в животноводстве и снижению риска передачи зоонозов человеку.
В статье представлены результаты исследования аллергенных свойств липосомальной формы гентамицина сульфата на лабораторных животных. В качестве тест - моделей для постановки коньюнктивальной пробы и реакции активной кожной анафилаксии были выбраны морские свинки, для реакциигиперчувствительности замедленного типа - белые мыши. Установлено отсутствие негативных эффектов на конъюнктиву глаз животных при использовании нативного препарата. Анафилактогенного эффекта не выявлено при сенсибилизации низкими дозами (71,3 мг/кг). При этом аллергизирующие свойства проявлялись при введении препарата в дозе 712,7 мг/кг, на что указывает статистически значимое увеличения эозинофилов крови у животных опытной группы в сравнении с контролем (19,0 ± 2,0 и 5,0 ± 1,0 прир < 0,004), а так же разница индекса реакций при постановке ГЗТ (7,3 ± 1,5 и 3,2 ± 0,4 % при р < 0,0001). Такие показатели могут свидетельствовать о возможности возникновения аллергической реакции при использовании высоких доз препарата и возможности развития гиперчувствительности IV типа, что необходимо учитывать в клинической практике.
Целью настоящего исследования явилась оценка фармакокинетического профиля препарата гемовит - плюс, представляющего собой комплекс органического соединения производного этилендиаминдиянтарной кислоты с биологически активными микроэлементами (Fe, Mn, Cu, Zn, Co, Se, I). Для эксперимента было отобрано 13 групп крыс по 3 животных в каждой (12 опытных и одна контрольная). Крысам опытных групп препарат гемовит - плюс вводили внутрижелудочно в дозе 13 мг / 1 кг массы тела животного. Далее через каждые два часа в течение суток проводили гуманную эвтаназию грызунов для отслеживания динамики изменения содержания микроэлементов в органах и тканях их организма. У крыс для исследования брали кровь, сердце, лёгкие, печень, почки, скелетную мускулатуру, толстый и тонкийотделы кишечника. Результаты эксперимента показали, что входящие в гемовит - плюс микроэлементы характеризуются высокой степенью биодоступности, достигая максимальных значений к 6-8 часу послевведения, что доказывает высокий уровень усвоения хелатной формы препарата.
В статье приведены результаты по оценке актопротекторных свойств препарата рутацирин на лабораторных животных. Для эксперимента из половозрелых нелинейных самцов крыс сформировали2 группы (опытную и контрольную) по 10 грызунов в каждой. Крысам опытной группы течение 7 дней(1 раз в сутки) внутрижелудочно вводили препарат рутацирин из расчета 1,2 г/кг массы тела в форме30%-ной суспензии. В контрольной группе животные получали эквиобъемное количество дистиллированной воды. Через неделю от начала введения препарата определяли общую физическую выносливость грызунов с помощью теста «вынужденное плавание с грузом». Сразу после тестирования у 5 животных из каждой группы отбирали кровь для лабораторных исследований. В результате установлено, что у лабораторных крыс опытной группы продолжительность плавания с грузом при дополнительной гипертермической нагрузке была больше контрольных значений на 19,78 % (р ≤ 0,05). Биохимические исследования крови крыс подтвердили адаптивное действие препарата, что проявилось улучшением маркеров энергетического обмена, состояния печени и окислительного стресса.
Статистика статьи
Статистика просмотров за 2026 год.
Издательство
- Издательство
- ВНИВИПФИТ
- Регион
- Россия, Воронеж
- Почтовый адрес
- ул. Ломоносова, 114Б
- Юр. адрес
- ул. Ломоносова, 114Б
- ФИО
- Паршин Павел Андреевич (Руководитель)
- E-mail адрес
- ermakova53@list.ru
- Контактный телефон
- +7 (908) 1376923
- Сайт
- https://nivipat.ru