Цель: оценить диагностическую ценность 20 биомаркеров при раке легкого и определить их информативность для возможного использования в клинической практике.
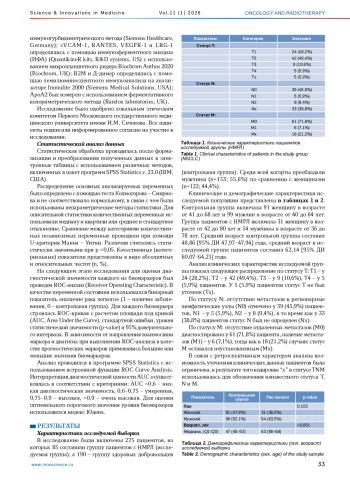
Материал и методы. В исследование были включены 85 пациентов с немелкоклеточным раком легкого (НМРЛ) и 190 здоровых добровольцев. Уровни биомаркеров определялись современными иммунологическими и биохимическими методами. Статистическая обработка включала U-критерий Манна – Уитни, а диагностическая ценность оценивалась по площади под ROC-кривой (AUC). Для оценки информативности маркеров с обратной ассоциацией проведен дополнительный ROC-анализ с инверсией переменной состояния. Определены пороговые значения биомаркеров с использованием индекса Юдена.
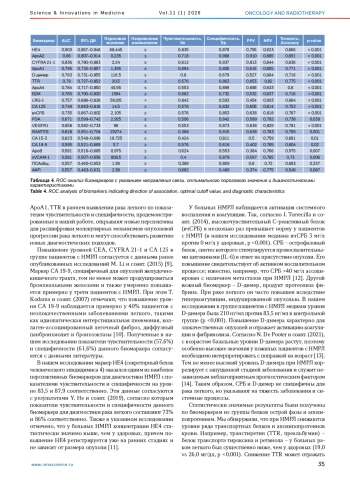
Результаты. У пациентов с НМРЛ отмечены статистически значимые изменения концентраций большинства исследованных биомаркеров с учетом строгой поправки Бонферрони: повышение уровней CEA, CA 125, HE4, B2M, вчСРБ, D-димер, CYFRA 21-1, LRG-1, а также снижение ApoA1, ApoA2, TTR, ApoA4, RANTES и VEGFR1. Наибольшие значения площади под кривой показали HE4 (0,903), ApoA2 (0,86), CYFRA 21-1 (0,836), ApoA1 (0,795), D-димер (0,793), TTR (0,79), ApoA4 (0,784), B2M (0,765), LRG1 (0,757).
Выводы. Отдельные биомаркеры крови демонстрируют высокие значения площади под кривой, что указывает на потенциал их применения с целью диагностики НМРЛ. Комплексное использование биомаркеров может повысить эффективность малоинвазивной диагностики рака легкого, что требует дальнейшего исследования. Для подтверждения полученных данных требуется валидация в многоцентровых исследованиях.
Идентификаторы и классификаторы
Рак легкого продолжает оставаться одной из наиболее актуальных проблем современной онкологии. Согласно данным проекта Всемирной организации здравоохранения «Глобальная онкологическая обсерватория» (The Global Cancer Observatory GCO), в 2022 году рак легкого занял лидирующее место в мире по показателям заболеваемости (2480675 новых случаев) и смертности от рака (1817469 летальных исходов) [1]. С биологической точки зрения, рак легкого характеризуется разнообразием морфологических типов, при этом на немелкоклеточный рак легкого (НМРЛ) приходится порядка 85% всех случаев заболевания [2].
Если у вас возникли вопросы или появились предложения по содержанию статьи, пожалуйста, направляйте их в рамках данной темы.
Список литературы
1. Zhou J, Xu Y, Liu J, et al. Global burden of lung cancer in 2022 and projections to 2050: incidence and mortality estimates from GLOBOCAN. Cancer Epidemiol. 2024;93:102693. DOI: 10.1016/j.canep.2024.102693
2. Molina JR, Yang P, Cassivi SD, et al. Non-small cell lung cancer: epidemiology, risk factors, treatment, and survivorship. Mayo Clin Proc. 2008;83(5):584-594. DOI: 10.4065/83.5.584 E
3. The state of oncological care for the population of Russia in 2022. Eds. Kaprin AD, Starinsky VV, Shakhzadova AO. M., 2022.
4. Ganti AK, Klein AB, Cotarla I, et al. Update of incidence, prevalence, survival, and initial treatment in patients with non-small cell lung cancer in the US. JAMA Oncol. 2021;7(12):1824-1832. DOI: 10.1001/jamaoncol.2021.4932
5. National Lung Screening Trial Research Team; Aberle DR, Adams AM, Berg CD, et al. Reduced lung-cancer mortality with low-dose computed tomographic screening. N Engl J Med. 2011;365(5):395-409. DOI: 10.1056/NEJMoa1102873 ▼ Контекст
6. Rykova EY, Ponomaryova AA, Zaporozhchenko IA, et al. Circulating DNA-based lung cancer diagnostics and follow-up: looking for epigenetic markers. Transl Cancer Res. 2018;7(Suppl 2):S153-S170. DOI: 10.21037/tcr.2018.02.08
7. Makar K, Wróbel A, Antczak A, Tworek D. Clinical utility of ctDNA analysis in lung cancer - a review. Adv Respir Med. 2025;93(3):17. DOI: 10.3390/arm93030017
8. Lee HJ, Kim YT, Park PJ, et al. A novel detection method of non-small cell lung cancer using multiplexed bead-based serum biomarker profiling. J Thorac Cardiovasc Surg. 2012;143(2):421-427. DOI: 10.1016/j.jtcvs.2011.10.046
9. Li Ma, Xiao-Wei Xie, Hai-Yan, et al. WangClinical evaluation of tumor markers for diagnosis in patients with non-small cell lung cancer in China. Asian Pac J Cancer Prev. 2015;16(12):4891-4894. DOI: 10.7314/apjcp.2015.16.12.4891
10. Kodama T, Satoh H, Ishikawa H, Ohtsuka M. Serum levels of CA19-9 in patients with nonmalignant respiratory diseases. J Clin Lab Anal. 2007;21(2):103-106. DOI: 10.1002/jcla.20136
11. He YP, Li LX, Tang JX, et al. HE4 as a biomarker for diagnosis of lung cancer: a meta-analysis. Medicine (Baltimore). 2019;98(39):e17198. DOI: 10.1097/MD.0000000000017198
12. Torrecilla JA, Scrimini S, Sauleda J. Role of C reactive protein in non-small cell lung cancer staging. Eur Respir J. 2014;38(Suppl 55):P2806. DOI: 10.1183/13993003/erj.38.Suppl_55.p2806
13. De Pooter N, Brionne-François M, Smahi M, et al. Age-adjusted D-dimer cut-off levels to rule out venous thromboembolism in patients with non-high pre-test probability: clinical performance and cost-effectiveness analysis. J Thromb Haemost. 2021;19(5):1271-1282. DOI: 10.1111/jth.15278
14. Li J, Yan S, Zhang X, et al. Circulating D-dimers increase the risk of mortality and venous thromboembolism in patients with lung cancer: a systematic analysis combined with external validation. Front Med (Lausanne). 2022;9:853941. DOI: 10.3389/fmed.2022.853941
15. Milaniuk A, Drabko K, Chojęta A. Role of albumin and prealbumin in assessing nutritional status and predicting increased risk of infectious complications during childhood cancer treatment. Acta Biochim Pol. 2024;71:13693. DOI: 10.3389/abp.2024.13693
16. Xu R, Wang J, Zhu Q, et al. Integrated models of blood protein and metabolite enhance the diagnostic accuracy for non-small cell lung cancer. Biomark Res. 2023;11:71. DOI: 10.1186/s40364-023-00497-2
17. Fujimoto Y, Inoue N, Morimoto K, et al. Significant association between high serum CCL5 levels and better disease-free survival of patients with early breast cancer. Cancer Sci. 2020;111(1):209-218.
Выпуск
Другие статьи выпуска
Представлен клинический случай лечения пациента с хроническим посттравматическим остеомиелитом бедренной кости. Принципиально важным моментом стал анализ результатов КТ-исследования в системе аппаратно-программного комплекса (АПК) «Автоплан» по разработанному способу и построение 3D-модели нижних конечностей. В результате был визуализирован очаг остеомиелита. На основе 3D-модели и интраоперационной навигации АПК «Автоплан» пациенту была выполнена секвестрнекрэктомия бедренной кости. Произведена оценка ближайших и отдаленных результатов лечения.
Послеоперационные вентральные грыжи являются одними из самых распространенных хирургических патологий во всем мире. Достижения медицинской науки за последние десятилетия позволили значительно улучшить результаты лечения данного заболевания вследствие обоснования и внедрения различных способов герниопластик с имплантацией синтетических эндопротезов. В то же время частота возникновения послеоперационных вентральных грыж остается на достаточно высоком уровне. На протяжении нескольких лет проводятся исследования, направленные на изучение молекулярных и клеточных механизмов формирования послеоперационных грыж. Ключевым вопросом в проблеме нарушения репарации тканей после лапаротомий является понимание процессов организации внеклеточного матрикса и активизации фибробластов. Внеклеточный матрикс предстает той уникальной средой, способствующей правильной структуризации коллагеновых волокон, приобретению прочности послеоперационного рубца и своевременной контракции раневой полости. Регуляция гомеостаза внеклеточного матрикса находится в зависимости от многих факторов, влияющих на сроки и полноценность репарации тканей после операционной травмы. Основной регенераторный потенциал составляют популяции фибробластов, ответственных за синтез и деградацию коллагена. Внеклеточный матрикс и фибробласты оказывают многофакторное влияние на репарацию раны, и нарушения баланса их взаимодействия может способствовать формированию послеоперационных вентральных грыж. Синтезируемые фибробластами молекулярные соединения, к которым относятся матричные металлопротеиназы, тканевые ингибиторы металлопротеиназ, а также актиновые и коллагеновые белки, играют важную роль как в заживлении операционной раны, так и в формировании грыж. Определение критических точек патогенеза послеоперационных вентральных грыж на молекулярном и клеточном уровнях позволит прогнозировать и профилактировать их образование. При этом открываются новые возможности для прецизионной стратификации пациентов перед оперативным лечением грыж и выбора персонифицированной хирургической тактики.
Цель: оценить влияние предоперационного введения ботулинического токсина типа А (БТА) на течение раннего послеоперационного периода у пациентов с большими послеоперационными вентральными грыжами (ПОВГ) в сравнении с контрольной группой.
Материал и методы. Проведен ретроспективный анализ 19 пациентов с ПОВГ класса W3 по классификации EHS. Основную группу (n=9) составили пациенты, получившие предоперационные инъекции БТА (Диспорт 900-1000 ЕД или Ксеомин 200 ЕД) в боковые мышцы живота под УЗ-контролем с последующей герниопластикой TAR. Контрольную группу (n=10) составили пациенты, оперированные без подготовки БТА (методы: TAR, Rives – Stoppa, TAR+bridge). Оценивались время операции, интенсивность болевого синдрома по ВАШ (визуально-аналоговая шкала) на первые, третьи и пятые сутки, продолжительность применения опиоидных анальгетиков, частота и структура осложнений, длительность госпитализации.
Результаты. В группе БТА интенсивность боли была достоверно ниже на первые сутки (медиана ВАШ 18,0 [11,5; 26,0] мм против 43,5 [40,0; 52,8] мм в контроле, p <0,001), на третьи сутки (11,0 [8,5; 13,0] мм против 41,5 [38,0; 42,8] мм, p <0,001) и на пятые сутки (2,0 [1,0; 3,5] мм против 31,5 [29,0; 33,0] мм, p <0,001). Общая частота осложнений в группе БТА составила 11,1% (гематома послеоперационной раны у одного пациента) против 70,0% в контроле (p=0,027), при этом инфекционные осложнения в группе БТА зафиксированы не были (0% против 40,0% в контроле, p=0,087). Медиана длительности госпитализации в группе БТА составила 8,0 [7,0; 8,0] дня против 9,0 [8,0; 15,8] дня в контроле (p=0,095).
Заключение. Предоперационная ботулинотерапия является безопасным и эффективным методом, достоверно снижающим интенсивность послеоперационной боли и частоту осложнений у пациентов с большими вентральными грыжами.
Предложена оригинальная методика реконструкции латеральной стенки аттика после раздельной аттикоантротомии, которая продемонстрирована на клиническом примере. Пациент П. (33 лет), диагноз: хронический левосторонний эпитимпаноантральный гнойный средний отит. Левосторонняя смешанная тугоухость 3 степени (костно-воздушный интервал 50–55 Дб). Под общей анестезией осуществлены ретроаурикулярный доступ в барабанную полость, раздельная аттикоантротомия, патологическое содержимое полостей среднего уха удалено, забор аутофасции, аутохряща. Пластинки хряща, согласно оригинальной методике, складывали вместе и прошивали рассасывающейся плетеной нитью из полиглактина 910 размер 4-0 с атравматичной иглой. Сначала прокалывали иглой по центру обе пластинки хряща спереди назад, выводили иглу и снова прокалывали рядом с предыдущим местом входа иглы сзади наперед, при этом сформированную петлю не затягивали, далее повторно прокалывали хрящ спереди назад рядом с предыдущим местом входа иглы с формированием второй петли, в которую продевали конец нити без иглы, после чего затягивали обе петли. Из наружного слухового прохода нить проводили через аттик в антрум и выводили в наружный слуховой проход. Сшитые пластины помещали в аттик так, чтобы своим торцом они прилежали к задней стенке наружного слухового прохода. Концы нитей затягивали пробным узлом так, чтобы сила натяжения нити прижимала хрящевые пластинки к задней стенке наружного слухового прохода. В месте прилегания узла к наружному краю задней костной стенки наружного слухового прохода делали метку, узел распускали, в области метки делали углубление-паз, концы нити повторно натягивали и завязывали узел в области углубления-паза. Реконструкция цепи слуховых косточек частичным протезом 2,25 мм, тимпанопластика фасцией и хрящом, ушивание раны, тампонада наружного слухового прохода. Через 1 год – костно-воздушный интервал 10 Дб, на компьютерной томографии височных костей рецидива холестеатомы нет, реконструкция латеральной стенки аттика состоятельна.
Заключение. Разработка и внедрение новых способов реконструкции в хирургии хронического гнойного среднего отита расширяет возможности и развивает компетенции врача. Предложенная методика формирования латеральной стенки аттика после раздельной аттикоатротомии позволяет эффективно восстановить анатомическое взаимоотношение среднего уха и наружного слухового прохода и имеет практическую значимость
Цель: разработать алгоритм, позволяющий выбрать оптимальный объем хирургического вмешательства больным метастатическим колоректальным раком, осложненным обтурационной кишечной непроходимостью.
Материал и методы. Исследование основано на анализе результатов лечения 202 пациентов метастатическим колоректальным раком, осложненным обтурационной кишечной непроходимостью, которые были разделены на две группы. В первую группу вошли 119 пациентов, которым первым этапом выполнено удаление первичного опухолевого очага. Вторую группу составили 83 пациента, которым выполнена только дренирующая симптоматическая операция, направленная на ликвидацию кишечной непроходимости.
Результаты. Показатель одногодичной летальности в первой группе составила 37 человек (31,1%), а во второй группе – 51 (61,4%) пациент. Многофакторный анализ выявил предикторы, влияющие на показатель одногодичной летальности: количество внутренних органов, пораженных метастазами, альбумин/глобулиновый коэффициент, лейкоцитарный индекс Кребса, индекс МСV, схема предстоящей таргетной терапии.
Заключение. Разработан этапный алгоритм принятия решения, позволяющий определить показания к удалению первичной опухоли, и создана программа ЭВМ для расчета риска одногодичной летальности больных метастатическим колоректальным раком.
Пациенты с местно-распространенным неоперабельным раком головы и шеи (РГШ) характеризуются неблагоприятным прогнозом и быстрым летальным исходом при стандартной системной химиотерапии и/или лучевой терапии. Медиана общей выживаемости при традиционном лечении не превышает 12–16 месяцев.
Цель: оценка долгосрочной выживаемости пациентов и эффективности селективной внутриартериальной химиотерапии (ВАХТ) при местнораспространенном неоперабельном РГШ.
Материал и методы. В открытое проспективное исследование были включены 56 пациентов с местно-распространенным неоперабельным РГШ (стадия IVA–IVB), которые получали селективную ВАХТ с использованием высоких доз Цисплатина и других химиопрепаратов с избирательным введением в артерии, питающие опухоль. Исследуемые пациенты были стратифицированы по локализации опухоли (ротоглотка, язык, дно полости рта, другие локализации), наличию лимфатических метастазов и сопутствующей патологии. Первичной конечной точкой был анализ общей выживаемости в среднесрочной перспективе (среднее наблюдение 39 месяцев, диапазон 10–221 месяц) наблюдения. Вторичными конечными точками стали ответ опухоли на лечение, безопасность процедуры, качество жизни.
Исходная когорта (n=56) характеризовалась такими показателями, как возраст 59,8 ± 9,8 года (41–81), мужчины 84,8% (n=47), женщины 15,2% (n=9). Основные факторы риска включали курение (69,7%, n=39), артериальную гипертензию (93,9%, n=52), сахарный диабет 2 типа (90,9%, n=51), атеросклероз брахиоцефальных артерий (54,5%, n=30). Средняя коморбидность составила 3,1±0,7 фактора риска на пациента, что отражало возраст и тяжесть популяции. Локализация первичной опухоли представлена ротоглоткой (24,2%), языком (21,2%), дном полости рта (16,1%), другими локализациями (39,4%). Наличие метастазов в регионарные лимфатические узлы выявлено у 51,5% пациентов (n=28). Большинство пациентов (90,9%, n=51) получило одну процедуру ВАХТ, меньшинство (9,1%, n=5) получило две или три процедуры.
Результаты. Из 56 исходно включенных пациентов на момент написания статьи (конец 2025 года) живы 33 пациента (58,9%, 95% ДИ: 44,7–72,6). Это составляет существенно более высокое значение по сравнению с ожидаемой выживаемостью при стандартном лечении, при котором этот показатель не превышает 15–20% через 24–39 месяцев. Средний ответ опухоли на лечение составил 7,9±5,4 по суррогатному показателю эффекта (диапазон: 3,2–31,9). Частота осложнений была низкой (12,1%, n=4), включала отек слизистой (n=1), гиперсаливацию (n=1), затекание контраста в соседние структуры (n=1), першение и чувство нехватки воздуха (n=1). Ни одного летального исхода, непосредственно связанного с процедурой ВАХТ, зафиксировано не было.
Заключение. Селективная внутриартериальная химиотерапия является эффективным и безопасным методом лечения для пациентов с местнораспространенным неоперабельным раком головы и шеи, существенно улучшающим долгосрочную выживаемость и качество жизни по сравнению со стандартным лечением. Результаты исследования подтверждают необходимость внедрения этого метода как стандартного подхода в лечении неоперабельных форм РГШ в специализированных учреждениях.
Цель: провести сравнительную оценку эффективности разработанного устройства для удаления инородных тел из мягких тканей.
Материал и методы. Для упрощения удаления инородных тел из мягких тканей, сокращения продолжительности и травматичности вмешательства была разработана малоинвазивная эндоскопическая система. Выполнено экспериментальное исследование в группах сравнения. Проводили моделирование огнестрельных пулевых слепых ранений на фрагменте свиного бедра (выстрелы из пистолета с дистанции 25 метров). В основной группе (20 шт.) удаление пуль осуществляли с применением разработанного устройства, в группе сравнения (20 шт.) – с применением зажима Граспера под ультразвуковым контролем. Оценивали продолжительность удаления пули с применением секундомера и травматичность манипуляции по количеству дополнительно удаленных мягких тканей.
Результаты. Продолжительность удаления пули в основной группе МЕД [Q1; Q3] 178,5 [148,5; 223,7] с была меньше, чем в группе сравнения – МЕД [Q1; Q3] 322,0 [248,5; 350,0] с (p=0,001). В основной группе вместе с пулями дополнительно было извлечено 9 фрагментов мышц, окружающих пули, в группе сравнения – 31 фрагмент. Травматичность вмешательства с использованием разработанного устройства в основной группе была ниже, чем в группе сравнения.
Заключение. Разработанное устройство для удаления инородных тел из мягких тканей позволяет снизить травматичность и сократить продолжительность экстракции предметов (в эксперименте). Применение в его составе эндоскопической визуализации совместно с ультразвуковой обеспечивает повышение точности позиционирования инородного тела в мягких тканях, а также способствует его захвату, надежному удержанию и малотравматичному удалению.
Цель: выявить потребности студентов в медико-профилактической помощи, определить барьеры доступа к медицинским услугам и оценить готовность к внедрению интегрированной модели «Университет здоровья» на примере РУДН им. Патриса Лумумбы.
Материал и методы. Проведено социологическое исследование методом анкетирования 682 студентов (489 российских, 193 иностранных) в возрасте 17–35 лет, распределенных по разным курсам, факультетам и направлениям подготовки. Использована авторская анкета из 60 вопросов с включением валидированного опросника EQ-5D-5L для оценки качества жизни.
Результаты. Большинство студентов (73,2%) оценили свое здоровье как хорошее и отличное. Однако значительное число обучающихся отметили сложности с психоэмоциональным здоровьем. Тревожные состояния отмечены у 44,7% студентов, среднее значение по шкале здоровья EQ-5D-5L составило 70,8±15,2 балла из 100. Ограниченная физическая активность наблюдается у 39,3% студентов, недостаточный сон характерен для 49,8% опрошенных. 89,4% студентов осведомлены о наличии Клинико-диагностического центра университета, однако обращались туда только 52,8%. Основными барьерами доступа являются организационные (длительное ожидание 20,1%, неудобное время 15,0%). 69,6% студентов положительно относятся к идее интегрированной модели «Университет здоровья» и 67,7% готовы активно использовать предлагаемые услуги.
Заключение. Исследование подтверждает необходимость развития интегрированной модели медико-профилактической помощи. Высокая готовность студентов к концепции «Университет здоровья» создает условия для успешной реализации этой модели в практике многопрофильного университета.
Современный этап технологической эволюции в здравоохранении характеризуется синергией медико-биологических наук и цифровых технологий, формирующей новую парадигму доказательной медицины. Генеративный искусственный интеллект (генИИ), обладающий потенциалом обработки гетерогенных данных и генерации предиктивных моделей, выступает ключевым драйвером персонализации медицинских услуг. В рамках данного исследования проведен многоуровневый анализ институциональных и технологических аспектов формирования научномедицинского кластера. Научно-медицинский образовательный кластер (НМОК) представляет собой перспективную организационно-экономическую модель, направленную на консолидацию ресурсов науки, образования, практического здравоохранения и бизнеса для достижения стратегических целей в области общественного здоровья.
Цель: изучить современные подходы к формированию научно-медицинских образовательных кластеров как инструмента решения стратегических задач в области охраны общественного здоровья и организации здравоохранения в регионе.
Материал и методы. В исследовании применены системный подход, метод контент-анализа данных научных исследований по проблеме, аналитический метод для оценки эффективности кластерной модели в условиях российских регионов.
Результаты. Выявлены ключевые системные ограничения: фрагментарность управления, дефицит кадров, управленческих компетенций и недостаточная ориентация научных разработок на приоритеты общественного здоровья. Определены проблемы формировании научно-медицинских образовательных кластеров в современных условиях и путей их решения.
Заключение. Формирование научно-медицинских кластеров выступает ключевым фактором развития инновационной экосистемы здравоохранения, обеспечивающей интеграцию академической науки, образовательных институтов, предпринимательского сектора и государственного регулирования. Ключевыми условиями успешности НМОК в регионе являются такие показатели, как лидирующая роль органа управления здравоохранением в координации всех участников кластера; ориентация на приоритеты общественного здоровья, определяемые на основе эпидемиологического анализа и данных мониторингов; интеграция образовательных программ в сфере управления искусственным интеллектом и экономики здравоохранения в деятельность кластера для подготовки кадров, способных работать в междисциплинарной среде; инвестиции в инновации с достигаемыми медико-демографическими и экономическими показателями.
Цель: выявить особенности гликозилирования белков при различных клинических формах рассеянного склероза.
Материал и методы. Изучены показатели гликома – интерлейкин-6 (IL- 6) и гликопротеин Р-селектин (SELP) у 135 больных с такими формами течения рассеянного склероза (РС), как ремиттирующий РС (РРС) – 71 больной, вторично-прогрессирующий РС (ВПРС) – 49 пациентов, первично-прогрессирующий РС (ППРС) – 15 пациентов. Использован ИФА-анализатор Multiscan FC при длине волны 450 нм с применением соответствующих диагностических наборов. Статистическая обработка проводилась с использованием критерия Манна – Уитни. Множественные сравнения групп различного течения РС проводились с помощью критерия Краскела – Уоллиса. Анализ корреляции выполнен на основе коэффициента ранговой корреляции Спирмена. Статистическая достоверность выводов определялась на 5% уровне значимости.
Результаты. В настоящем исследовании была предпринята попытка выявления зависимости уровня IL-6 и SELP от формы, длительности течения и тяжести РС, что выявило только значимую связь SELP с длительностью течения заболевания для РРС. Данных о связи этих показателей с возрастом и полом пациентов получено не было.
Выводы. Показана определенная специфичность изменений гликозилирования белков при рассеянном склерозе, что позволяет использовать их в качестве маркеров для диагностики различных форм рассеянного склероза и сходных с ним заболеваний. Хотя в проведенном исследовании была выявлена значимая связь только у SELP и только с длительностью заболевания при ремиттирующей форме РС, не исключена возможность получения дополнительных результатов при увеличении количества включенных в исследование пациентов, а также при включении в исследование других показателей гликома.
Обоснование. В связи с широким распространением вируса SARS-CoV-2 в мире и в России, его постоянными мутациями, а также нестойким поствакцинальным и постинфекционным иммунитетом у населения, в настоящее время сохраняется эпидемический потенциал новой коронавирусной инфекции (COVID-19). Опыт пандемии продемонстрировал высокую летальность среди больных COVID-19 с острым коронарным синдромом (ОКС), в частности, от инфаркта миокарда (ИМ).
Цель: на основании лабораторно-инструментальных особенностей течения COVID-19 у больных с ОКС разработать модель прогнозирования развития ИМ у данной категории больных.
Материал и методы. В открытое проспективное нерандомизированное исследование были включены 104 пациента с ОКС на фоне тяжелого течения COVID-19, госпитализированных в 2022 году. Для решения задачи прогнозирования ИМ среди пациентов были сформированы группы наблюдения: группа 1 (n=35) – пациенты с нестабильной стенокардией (НС) и группа 2 (n=69) – с ИМ. Всем пациентам проводился круглосуточный мониторинг витальных функций с помощью прикроватного монитора в динамике. Исследовались лабораторные (общеклинические, биохимические) показатели, уровень цитокинов (интерлейкины:1b, 2, 4, 6, 10, интерферон γ, фактор некроза опухоли α); инструментальные (КТ органов грудной клетки, ЭхоКГ); рассчитывали баллы по шкалам SOFA (Sepsis-related Organ Failure) и SAPS II (Simplified Acute Physiology Score). Статистическая обработка данных выполнена в среде пакета SPSS 25.0. Выполняли математическое моделирование с помощью многомерной логистической регрессии. Проводили анализ характеристических кривых (ROC-кривых) в предсказанной в многомерной модели вероятности развития ИМ. Результаты считали статистически значимыми при р<0,05. По полученным данным была построена многомерная модель методом логистической регрессии с пошаговым включением или исключением предикторов по алгоритму Вальда.
Результаты. В прогностическую модель вошли баллы по шкале SAPS II, цитокины (интерферон гамма, фактор некроза опухоли альфа) и степень поражения легких по данным компьютерной томографии. В ходе проведенного анализа установлено, что разработанная математическая модель оценки риска развития ИМ у больных с ОКС на фоне тяжелой формы COVID-19, созданная методом многомерной логистической регрессии, обладает чувствительностью 98,6% и специфичностью 85,7%.
Выводы. Установлены ранние предикторы развития ИМ у пациентов с ОКС на фоне COVID-19: степень поражения легких по данным КТ, количество баллов по шкале SAPS II, уровни цитокинов (интерферона и фактора некроза опухоли). На основании данных предикторов разработана математическая модель, позволяющая прогнозировать ИМ на фоне тяжелой формы COVID-19.
Статистика статьи
Статистика просмотров за 2026 год.
Издательство
- Издательство
- СамГМУ
- Регион
- Россия, Самара
- Почтовый адрес
- 443099, Приволжский федеральный округ, Самарская область, г. Самара, ул. Чапаевская, д. 89
- Юр. адрес
- 443099, Приволжский федеральный округ, Самарская область, г. Самара, ул. Чапаевская, д. 89
- ФИО
- Колсанов Александр Владимирович (ректор)
- E-mail адрес
- info@samsmu.ru
- Контактный телефон
- +7 (846) 3741001
- Сайт
- https://samsmu.ru/